
【题目】按要求完成下列表格。
序号 | 物质 | 杂质 | 除去杂质试剂及方法、化学方程式 |
(1) | KOH溶液 | K2CO3 | _____ |
(2) | CO2气体 | HCI | _____ |
(3) | KNO3固体 | NaCl | _____ |
【答案】加入适量的氢氧化钙溶液,过滤,![]() 通入饱和碳酸氢钠溶液中,
通入饱和碳酸氢钠溶液中,![]() 可加热水溶解,制成热的饱和溶液,然后降温结晶,然后过滤
可加热水溶解,制成热的饱和溶液,然后降温结晶,然后过滤
【解析】
(1)加适量氢氧化钙溶液,碳酸钾与氢氧化钙反应生成碳酸钙和氢氧化钾,过滤,除去碳酸钙,该反应的化学方程式为:![]() 。
。
(2)可将混合气体通入饱和碳酸氢钠溶液中,碳酸氢钠与HCl反应生成氯化钠、二氧化碳和水,可除去氯化氢气体,该反应的化学方程式为:![]() ;
;
(3)硝酸钾的溶解度随温度的升高而增大,且受温度影响较大,氯化钠的溶解度随温度升高而增大,受温度影响较小,可加热水溶解,制成热的饱和溶液,然后降温结晶,然后过滤。
故填:
序号 | 物质 | 杂质 | 除去杂质试剂及方法、化学方程式 |
(1) | KOH溶液 | K2CO3 | 加入适量的氢氧化钙溶液,过滤, |
(2) | CO2气体 | HCl | 通入饱和碳酸氢钠溶液中, |
(3) | KNO3固体 | NaCl | 可加热水溶解,制成热的饱和溶液,然后降温结晶,然后过滤 |


 天天向上口算本系列答案
天天向上口算本系列答案科目:初中化学 来源: 题型:
【题目】下列所示的图像能反映相对应实验的是( )
A. 向pH=12的Ca(OH)2溶液中不断加水稀释
向pH=12的Ca(OH)2溶液中不断加水稀释
B. 向碳酸钙固体中逐滴加入稀盐酸至过量
向碳酸钙固体中逐滴加入稀盐酸至过量
C. 在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
在40℃,将饱和的硝酸钾溶液恒温蒸发水分至有白色晶体析出
D. 将足量的金属镁片和锌片分别和等质量的相同质量分数的稀硫酸混合
将足量的金属镁片和锌片分别和等质量的相同质量分数的稀硫酸混合
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据图示的反应情况,判断下列说法中不正确的是( )

A.部分反应物没有参与反应。
B.发生的反应属于复分解反应
C.生成两种产物的质量比为22:7
D.反应过程中参加反应的NO破裂成了原子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知:含有碳、氢元素的有机物在氧气中完全燃烧,产生二氧化碳和水。某混合气体在氧气中完全燃烧后的产物依次通过浓硫酸和氢氧化钠溶液,经完全吸收后,测得浓硫酸和氧氧化钠溶液增重的质量比为9:11,则该气体的可能组合是( )
①CH4 ②CO ③C2H2 ④C2H4 ⑤H2
A.①②③
B.①③④
C.①②⑤
D.②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列图①~④分别与相应的操作过程相对应,其中正确的是
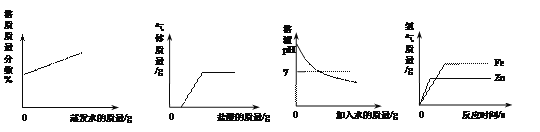
① ② ③ ④
A.①在恒温的条件下,将足量的氯化钠饱和溶液蒸发适量的水分
B.②向露置在空气中部分变质的氢氧化钠溶液中加入稀盐酸
C.③向氢氧化钠溶液中不断加水稀释
D.④相同质量的且过量的锌粉和铁粉,分别与质量和质量分数相同的稀盐酸反应
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:


氯化铵和硫酸钠的溶解度随温度变化如上图所示。回答下列问题:
(1)欲制备10.7gNH4Cl,理论上需NaCl_____g。
(2)实验室进行蒸发浓缩用到的主要仪器有_____、烧杯、玻璃棒、酒精灯等。
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为_____。
(4)不用其他试剂,检查NH4Cl产品是否纯净的方法及操作是_____。
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】锂广泛应用于电池、贮氢等领域,锂在化合物中显+1价。图中A为周期表中锂元素的信息,其余为四种粒子的结构示意图。

(1)从图A中数值获得锂的核电荷数为_____。
(2)B、C、D、E中,属于同种元素的是_____(填编号);D结构示意图对应的化学符号为_____。
(3)LiMnO2是一种电极材料,其中Mn的化合价为_____。
(4)用化学符号表示:①两个锂原子:_____;②氢氧化锂:_____。
(5)如图为元素周期表的一部分,X、Y、Z代表三种不同元素,以下_____判断正确。
He | |||
X | |||
Y | Z |
A 原子序数:Z>Y
B 核外电子数:X=Y
C Y和Z处于同一周期
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】次氯酸钙[Ca(ClO)2]是漂白粉的主要成分之一,可用于杀菌消毒。用消石灰制备次氯酸钙的主要工艺流程如下:

(1)NaClO中氯元素的化合价是______。
(2)处理器中发生的复分解反应的化学方程式是______。
(3)上述流程中,只涉及到物理变化的设备有______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是实验室常用的实验装置,请回答下列问题

(1)仪器①的名称是 _____。
(2)实验室用 A 装置制取 O2,请写出有关化学反应方程式__________;可用 D 装置收集氧气,其原理是 _____。
(3)实验室制取并收集 CO2,选用的装置组合为 _____(填字母)。在添加药品前,应先进行的操作是_________,若用装置 C 干燥 CO2,气体由导管_________端(填“a”或“b”)通入。
(4)某学校研究小组为探究氢氧化钠与二氧化碳的反应,在室温为 15℃时,同学们将 10g 氢氧化钠固体完全溶解溶于 80g 水中,然后匀速的通入二氧化碳气体,同时用传感器测定溶液的 pH 变化,数据采集器记录并绘制的图像如下图所示。(资料链接:Na2CO3+ CO2+H2O= 2NaHCO3)


①如图甲所示实验中,用“分液漏斗”而不用“长颈漏斗”的原因是 _____;
②乙图中 M 点发生的主要化学反应方程式为 _____;
③请写出乙图 N 点对应溶液中的溶质 _____;
④上述实验能得出的结论是 _____(填序号)。
a.碳酸氢钠溶液显碱性
b.若往 NaOH 溶液不断通入 CO2 至过量,溶液最终呈酸性
c.相同浓度的 Na2CO3 溶液和 NaHCO3 溶液,碱性大小关系为:Na2CO3> NaHCO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com