取10克含有杂质氯化钠的碳酸钠样品溶于水后,滴加氯化钙溶液至不再生成沉淀为止,得到沉淀9克.求样品中杂质的质量分数.
解:设样品中碳酸钠的质量为x.
Na
2CO
3+CaCl
2=2NaCl+CaCO
3↓
106 100
x 9g
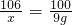
解之得:x=9.54g
样品中杂质的质量分数为:
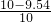
×100%=4.6%
答:样品中杂质的质量分数为4.6%.
分析:碳酸钠和氯化钙溶液反应生成碳酸钙沉淀,可由碳酸钙的质量,根据化学方程式求出碳酸钠的质量,进而求出杂质的质量和质量分数.
点评:根据化学反应方程式计算的过程中,一定要注意:(1)设未知量x时,x的后面不要带单位;(2)书写化学方程式的时候,切记严格地按照“写→配→标→注”步骤细心书写;(3)找质量关系时,最好先找下一行的实际质量关系(即已知量和未知量),然后再对应着找上一行的相对质量关系.并且,切记将它们都写在相应的化学式的正下方,分居上下两行.(4)列比例式时,要按照“上一行的相对质量比等于下一行的实际质量比”的顺序来列;保证是对应比相等.(5)求算x时,可以参考着化学方程式下面的两行质量关系中的上下或左右的倍数关系来求算.当没有倍数关系时,再按照一般的方法来求算便是.(6)在写答案时,只需要简明扼要地答出关键语句即可.

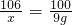
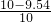 ×100%=4.6%
×100%=4.6%
