
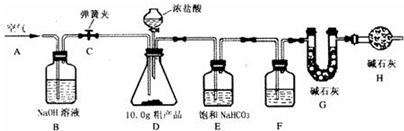
已知某纯碱粗产品仅含有NaCl杂质,为测定该纯碱粗产品中纯碱的质量分数,某兴趣小组的同学设计了下图所示的实验装置,取10.0 g粗产品进行实验。

【说明】碱石灰是CaO与NaOH 的固体混合物,能吸收水和二氧化碳。E装置中的饱和NaHCO3溶液是为了除去二氧化碳气体中的氯化氢,发生的反应为NaHCO3 十HC1 = NaCl十CO2↑十H2O。
实验主要操作步骤如下:
①连接好装置,检查气密性;②打开弹簧夹C,在A处缓缓通入一段时间空气;③称量 G的质量;④关闭弹簧夹C,慢慢滴加浓盐酸至过量,直至D中无气泡冒出;⑤打开弹簧夹C,再次缓缓通入一段时间空气;⑥再次称量 G的质量,测得质量增加了0.48 g。
请回答下列问题
(1)F中的试剂应为___________________________。
(2)B装置的作用是__________________________,B装置中发生反应的化学方程式为:
___________________________________________________________________________
(3)H装置的作用是 。
(4)事实上10.0 g粗产品只能产生0.40g CO2。请你仔细分析上述实验,解释G的质量增加了0.48 g的原因(假设操作均正确) 。
 字词句段篇系列答案
字词句段篇系列答案科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源:2012年中考化学模拟试卷(40)(解析版) 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com