
 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:初中化学 来源: 题型:
过氧化钠(Na2O2)是潜水艇氧气再生装置中制氧剂,它是一种淡黄色粉
末,能与二氧化碳反应生成氧气,反应的化学方程式是2Na2O2+2CO2=O2+2X,
则Na2O2中氧元素化合价为__________,X的化学式为_________________。①②NaHCO3
查看答案和解析>>
科目:初中化学 来源: 题型:
如右图所示,小田同学在
进行酸碱中和反应的实验时,向烧杯中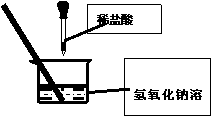
的氢氧化钠溶液滴加稀盐酸一会儿后,
发现忘记了滴加指示剂,导致无法判断该中和反应
进行的程度。于是他对所得的溶液的酸碱性进行探究。
【探究目的】探究所得溶液的酸碱性。
【提出猜想】所得溶液可能呈 碱性,也可能呈_______性,还可能呈______性。
碱性,也可能呈_______性,还可能呈______性。
写出该中和反应的化学方程式_______________________________
[实验验证]
| 实验操作 | 实验现象 | 结论 |
| 用试管取溶液1-2ml,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变_______ | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈_______________ |
[分析与思考] ① 若溶液呈碱性,则溶液中使其呈碱性的离子是_____(填写离子符号)
② 若无色酚酞试液不变色,为了进一步确定溶液的酸碱性,小田提出了以下方案:方案一:取样,加入碳酸钠溶液,若观察到______________,则所取溶液呈酸性,若无明显现象,则呈中性
方案二:取样,加入金属锌 ,若____________,则所取溶液呈酸性,该反应的化学方程式为_____________________________,若无明显现象,则呈中 钠易与氧气反应变质
,若____________,则所取溶液呈酸性,该反应的化学方程式为_____________________________,若无明显现象,则呈中 钠易与氧气反应变质
查看答案和解析>>
科目:初中化学 来源: 题型:
实验室制取下列气体:①用锌和稀硫酸制取氢气;②用双氧水和二氧化锰制取氧气;③用石灰石和稀盐酸制取二氧化碳气体。下列有关说法正确的是:( )
A.反应②需要对气体发生装置加热 B.都可以用向下排空气法收集气体
C.都可以用向上排空气法收集气体 D.都可以用相同的发生装置
查看答案和解析>>
科目:初中化学 来源: 题型:
2010年在中国的上海举行世博会,下列措施不符合世博会“节能、环保、低碳”理念的是:( )
A.“阳光谷”上采阳光、下蓄雨水,可给世博园区提供照明用电和生活用水
B.主题馆的东、西两墙种植大面积的生态植物,以吸收二氧化碳
C.用煤发电,以保证充足的电力供应
D.在交通、建筑、生活设施等方面广泛应用新能源技术,以减少化石燃料的使用
查看答案和解析>>
科目:初中化学 来源: 题型:
以下是某同学做过的小实验,其中能成功的是
① 用蜡烛制取少量的炭黑 ② 用碎鸡蛋壳和食醋制取少量CO2
③ 用肥皂水区别硬水和软水 ④ 用淬火后的缝衣针制作钓鱼钩
A.②③ B.①②③ C.②③④ D.①②③④
查看答案和解析>>
科目:初中化学 来源: 题型:
K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备K2SO4和Mn3O4的工艺流程如下:
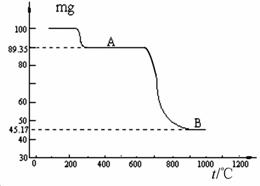
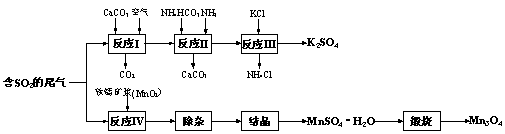
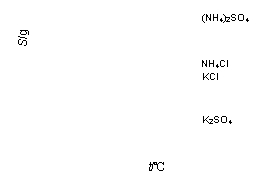
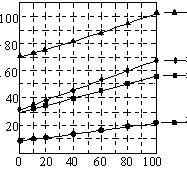
图1 图2
(1)反应Ⅰ中所需碳酸钙为粉末状,其目的是 ;反应生成了硫酸钙和二氧化碳,请写出反应的化学方程式 。
反应Ⅱ中要得到纯净的碳酸钙的操作为: 、洗涤、 。操作中若不进行洗涤处理,则制得的碳酸钙中一定含有 杂质。
(2)几种盐的溶解度如图1。反应III中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行蒸发结晶、 、洗涤、干燥等操作即得K2SO4产品。反应Ⅲ中有硫酸钾析出而没有氯化铵析出的原因是 。反应Ⅲ所得到的溶液为硫酸钾的 (填“饱和”或“不饱和”)溶液。
(3)检验K2SO4样品是否含有氯化物杂质的实验操作是: 。
A.取样溶解静置,向溶液中滴加硝酸银溶液,若无白色沉淀生成,则无氯化物;
B.取样溶解静置,先向溶液中滴加过量氯化钡溶液,静置后向上层溶液中滴加硝酸银溶液,若无白色沉淀生成,则无氯化物;
C.取样溶解静置,先向溶液中滴加过量硝酸钡溶液,静置后向上层溶液中滴加硝酸银溶液,若无白色沉淀生成,则无氯化物;
(4)反应Ⅰ到反应Ⅲ的过程中可循环利用的物质是 。
(5)Mn3O4中锰元素的化合价为+2和+3,Mn3O4与稀硫酸反应的化学方程式为 。
(6)图2是煅烧MnSO4•H2O时温度与剩余固体质量变化曲线。
①该曲线中A段所表示物质的化学式为 。
②煅烧过程中固体锰含量随温度的升高而增大,当温度超过1000℃时,得到二氧化硫和一种相对稳定的物质Mn3O4,请写出A段的物质转化为Mn3O4的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com