
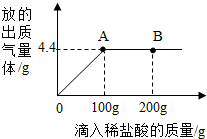
 在一烧杯中盛有20gNaCl和Na2CO3组成的固体混合物,加100g水溶解,制成溶液,向其中逐渐滴加溶质质量分数为7.3%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示.
在一烧杯中盛有20gNaCl和Na2CO3组成的固体混合物,加100g水溶解,制成溶液,向其中逐渐滴加溶质质量分数为7.3%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系曲线如图所示.分析 (1)碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,据此写出化学方程式即可;
(2)由图示可知,当滴加稀盐酸至图中A点时,反应已完全,故滴加稀盐酸至图中B点时,盐酸有剩余.盐酸是酸,酸的ph值<7;
(3)根据碳酸钠与盐酸反应的化学方程式和HCl的质量,列出比例式,就可计算出参加反应的碳酸钠的质量、反应生成的氯化钠的质量和生成的二氧化碳的质量.进而计算出溶质质量和溶液质量,然后根据溶质质量分数=$\frac{溶质质量}{溶液质量}$×100%计算即可.
解答 解:(1)由图示可知,当滴加稀盐酸至图中A点时,气体不再增加,说明碳酸钠已完全反应;故填:A;
(2)由图示可知,当滴加了100g稀盐酸时,放出气体的总质量为4.4g.故填:4.4;
(3)当滴加稀盐酸至图中A点时,烧杯中溶液的总质量为:20g+100g+100g-4.4g=215.6g;故填:215.6;
(4)设参加反应的碳酸钠的质量为x,反应生成的氯化钠的质量为y.
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 117 44
x y 4.4g
∴$\frac{106}{x}=\frac{117}{y}=\frac{44}{4.4g}$,
解之得:x=10.6g,y=11.7g,
烧杯里不饱和溶液中溶质的质量为:11.7g+(20g-10.6g)=21.1g,
答:其中溶质的质量为21.1g.
点评 本题主要考查学生运用化学方程式和溶质质量分数公式进行计算的能力.考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.


 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:初中化学 来源: 题型:解答题
| 操作 | 恒温加入5g硝酸钾 | 恒温蒸发5g水 | 降温到t1℃ | 恒温加入20g10%的硝酸钾溶液 |
| 溶质质量/g | 10g | 7.5g | 2g | 12g |
| 溶质质量分数/g | 50% | 50% | 16.7% | 30% |
| 溶解度/g | 100g | 100g | 20g | 100g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
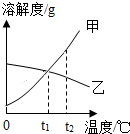 如图是两种物质的溶解度曲线,下列说法正确的是 ( )
如图是两种物质的溶解度曲线,下列说法正确的是 ( )| A. | 甲的溶解度大于乙的溶解度 | |
| B. | t2℃时等质量甲、乙两物质的饱和溶液降温至t1℃时,两溶液中溶质质量分数相等 | |
| C. | t1℃时等质量甲、乙两种物质的饱和溶液中溶质质量相等 | |
| D. | 甲物质中混有少量的乙物质适合蒸发结晶的方法提纯甲 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
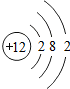 某粒子结构示意图如图所示,下列对该粒子的判断中,正确的是( )
某粒子结构示意图如图所示,下列对该粒子的判断中,正确的是( )| A. | 该粒子原核内有12个质子 | B. | 该粒子是阴离子 | ||
| C. | 该粒子在化学变化中易得电子 | D. | 该粒子属于非金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 元素符号 | 离子结构示意图 | 离子符号 | 它们组成的单质相互反应的化学方程式 |
| Al | O2- | Al3+ | 4Al+3O2$\frac{\underline{\;点燃\;}}{\;}$2Al2O3 |
| 铝元素 | 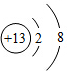 | 铝离子 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气参加的化学反应都是化合反应 | |
| B. | 液态氧用于火箭发动机,以促使燃料迅速燃烧 | |
| C. | 氧气的化学性质比较活泼,可与许多金属与非金属反应 | |
| D. | 在钢铁冶炼中,吹入富氧空气可以提高炉温,加速冶炼过程 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com