
| A、①②显酸性,③④显碱性 | B、c(NH4+):④<③<② | C、溶液的pH:①<②<④ | D、②溶液中:c(NH4+)+c(H+)=c(SO42-)+c(OH-) |


科目:初中化学 来源:甘肃省兰州四中2012届九年级上学期期中考试化学试题 题型:058
“用双氧水和二氧化锰制氧气”的实验,某同学做了该实验后,展开了下列思考与探究:
(1)催化剂MnO2的用量对反应速率有没有影响呢?他做了这样一组实验:每次均用30 mL 10%的H202溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500 mL氧气时所用的时间,结果如下:(其他实验条件均相同)

请分析表中数据回答:MnO2的用量对反应速率有没有影响呢?如果有,是怎样影响的呢?
答:___________________.
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?他又做了一组实验:每次均取5 mL 30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验,每次所用二氧化锰的质量均为0.2克.记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
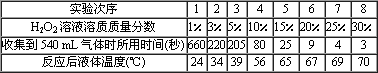
请分析表中数据回答:H2O2溶液的溶质质量分数对反应速率有没有影响呢?如果有,是怎样影响的呢?
答:__________________.
由表中数据还可看出,该反应是个________(填“放热”或“吸热”)反应.
(3)还有哪些因素可能影响该反应的速率呢?
请说出你的一个猜想:________.
查看答案和解析>>
科目:初中化学 来源:2012届甘肃省兰州四中九年级上学期期中考试化学试卷(带解析) 题型:问答题
“用双氧水和二氧化锰制氧气”的实验,某同学做了该实验后,展开了下列思考与探究:(1)催化剂MnO2的用量对反应速率有没有影响呢?他做了这样一组实验:每次均用30mL10%的H202溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(克) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间(秒) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| 收集到540mL气体时所用时间(秒) | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
| 反应后液体温度(℃) | 24 | 34 | 39 | 56 | 65 | 67 | 69 | 70 |
查看答案和解析>>
科目:初中化学 来源:2011-2012学年甘肃省九年级上学期期中考试化学试卷(解析版) 题型:简答题
“用双氧水和二氧化锰制氧气”的实验,某同学做了该实验后,展开了下列思考与探究:(1)催化剂MnO2的用量对反应速率有没有影响呢?他做了这样一组实验:每次均用30mL10%的H202溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
|
实验次序 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
|
MnO2粉末用量(克) |
0.1 |
0.2 |
0.3 |
0.4 |
0.5 |
0.6 |
0.7 |
0.8 |
0.9 |
1.0 |
|
所用时间(秒) |
17 |
8 |
7 |
5 |
4 |
3 |
2 |
2 |
2 |
2 |
请分析表中数据回答:MnO2的用量对反应速率有没有影响呢?如果有,是怎样影响的呢?
答:________________________________________________。
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?他又做了一组实验:每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验,每次所用二氧化锰的质量均为0.2克。记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
|
实验次序 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
|
H2O2溶液溶质质量分数 |
1% |
3% |
5% |
10% |
15% |
20% |
25% |
30% |
|
收集到540mL气体时所用时间(秒) |
660 |
220 |
205 |
80 |
25 |
9 |
4 |
3 |
|
反应后液体温度(℃) |
24 |
34 |
39 |
56 |
65 |
67 |
69 |
70 |
请分析表中数据回答:H2O2溶液的溶质质量分数对反应速率有没有影响呢?如果有,是怎样影响的呢?
答:____________________________________。
由表中数据还可看出,该反应是个__________(填“放热”或“吸热”) 反应。
(3)还有哪些因素可能影响该反应的速率呢?
请说出你的一个猜想:__________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
水和溶液在生命活动和生产、生活中起着十分重要的作用。
(1)为了防止水的污染,下列做法中,有利于保护水资源的是______(填序号)。
①抑制水中所有动、植物生长; ②不任意排放工业废水;
③大量使用化肥农药; ④生活污水经过净化处理后再排放。
(2)从组成角度看:水是由___________组成的 。
(3)根据下图,回答问题。

|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|

|
|
|
|
|
|
|

|


硝酸钾、氯化钠、氢氧化钙的溶解度曲线
①交点P的含义是_____。
②随温度升高,氢氧化钙溶解度的变化趋势是_____。
③如图所示,小烧杯中分别取等质量的三种物质的饱和溶液,分别放入装有等质量水的大烧杯中, 若向大烧杯中的水(室温)中加入等质量的硝酸铵使之充分溶解。
下列关于该实验的说法中,正确的是____(填字母序号)。
|

 |
 |

 | ||||||||||||
| 甲 | 乙 | 丙 |
A. 甲、乙的小烧杯中有晶体析出,丙的小烧杯中变浑浊
B. 整个过程中,三只小烧杯中溶剂的质量不变
C. 80℃时,硝酸钾溶液的浓度一定大于氯化钠溶液的浓度
D. 整个过程中,三种物质的溶液均为饱和溶液
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
“用双氧水和二氧化锰制氧气”的实验,某同学做了该实验后,展开了下列思考与探究:(1)催化剂MnO2的用量对反应速率有没有影响呢?他做了这样一组实验:每次均用30mL10%的H202溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(克) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间(秒) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
请分析表中数据回答:MnO2的用量对反应速率有没有影响呢?如果有,是怎样影响的呢?
答:________________________________________________。
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?他又做了一组实验:每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数的溶液进行实验,每次所用二氧化锰的质量均为0.2克。记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| 收集到540mL气体时所用时间(秒) | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
| 反应后液体温度(℃) | 24 | 34 | 39 | 56 | 65 | 67 | 69 | 70 |
请分析表中数据回答:H2O2溶液的溶质质量分数对反应速率有没有影响呢?如果有,是怎样影响的呢?
答:____________________________________。
由表中数据还可看出,该反应是个__________(填“放热”或“吸热”) 反应。
(3)还有哪些因素可能影响该反应的速率呢?
请说出你的一个猜想:__________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com