
| 实验方案 | 测溶液pH | 滴加Na2CO3溶液 | 滴加BaC12溶液 |
| 实验操作 | 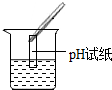 | 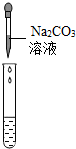 | 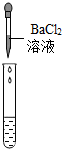 |
| 实验现象 | 试纸变色,对比标准比色卡,pH<7 | 产生无色气泡有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |
分析 【学生板演】硫酸和氢氧化钠反应生成硫酸钠和水,注意化学式的写法和配平;
【假设猜想】根据酸碱不能共存判断不合理的猜想;
【实验探究】根据碳酸钠和硫酸反应能生成二氧化碳气体解答;
【评价反思】①根据图示操作判断,检测溶液的pH时,pH试纸不能伸入溶液中;
②检验一种物质时要排除其他物质的干扰,硫酸钠也能与氯化钡反应生成白色沉淀
解答 解:【学生板演】硫酸和氢氧化钠反应生成硫酸钠和水,化学方程式为H2SO4+2NaOH═Na2SO4 +2H2O;
【假设猜想】硫酸和氢氧化钠反应生成硫酸钠和水,酸或碱可能过量,但不能同时过量,因为酸碱不能共存,会继续反应,故猜想四不合理;
【实验探究】(3)由于氢氧化钠与硫酸铜反应生成氢氧化铜蓝色沉淀,所以滴加几滴CuSO4溶液,无明显变化,溶液中一定没有氢氧化钠;
(4)由于溶液显酸性,伸入pH试纸后会变色,对比比色卡,pH<7;碳酸钠和硫酸反应能生成二氧化碳气体,会看到溶液中有气泡冒出;
【评价反思】①根据图示操作判断,检测溶液的pH时,pH试纸不能伸入溶液中,应用玻璃棒蘸取少量溶液涂到pH试纸上;
②检验一种物质时要排除其他物质的干扰,硫酸钠也能与氯化钡反应生成白色沉淀,故不能证明溶液中一定存在硫酸;
该方案中稀硫酸与碳酸钠发生反应生成了硫酸钠、水和二氧化碳,其反应方程式为:Na2CO3+H2SO4═Na2SO4+H2O+CO2↑
故答案为:
【学生板演】H2SO4+2NaOH═Na2SO4+2H2O;
【假设猜想】猜想四或四;
【实验探究】
(1)NaOH或氢氧化钠;
(2)试纸变色,对比比色卡,pH<7; 有气泡产生;
【评价反思】Na2CO3+H2SO4═Na2SO4+H2O+CO2↑.
点评 此题通过中和反应考查了化学方程式的书写,实验方案设计、实验操作以及实验方案的评价,解答时要全面审题,认真解答.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 盐酸溶液浓度 | 反应开始时酸 溶液的温度 | 反应开始到2分钟产生的气体体积 | 反应结束共产生气体体积 |
| 5% | 20℃ | 10mL | 60mL |
| 10% | 20℃ | 19mL | 118mL |
| 15% | 20℃ | 28mL | 175mL |
| 5% | 35℃ | 28mL | 60mL |
| 10% | 35℃ | 72mL | 118mL |
| 15% | 35℃ | 103mL | 175mL |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
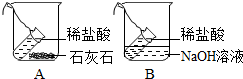 小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究.
小刚和小洁以“化学反应中,反应物和生成物的质量关系”为课题进行科学探究.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
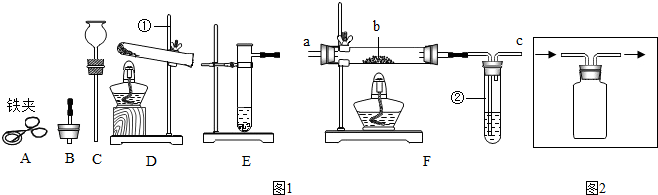
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
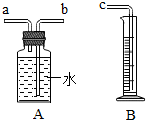 某同学为比较锌、铁、铝的金属活动性强弱.
某同学为比较锌、铁、铝的金属活动性强弱.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
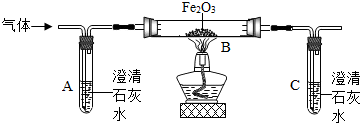 蚊虫叮咬分泌出蚁酸刺激皮肤,某兴趣小组对蚁酸进行如下探究.
蚊虫叮咬分泌出蚁酸刺激皮肤,某兴趣小组对蚁酸进行如下探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com