
 硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.
硫酸和盐酸既是实验室常用的试剂,也是重要的化工原料.分析 (1)依据两种酸的做成情况分析;
(2)根据两种酸是否具有挥发性分析即可;
(3)根据两种酸根离子的鉴别方法分析;
(4)通过计算相同质量的氢氧化钙消耗H2SO4和HCl的关系得出结论.
解答 解:(1)硫酸和盐酸都属于酸,两者的不同主要是酸根的不同;
(2)由于浓盐酸具有强烈的挥发性而浓硫酸没有,所以打开两瓶分别盛有浓硫酸和浓盐酸的试剂瓶,瓶口出现白雾的是浓盐酸;
(3)硫酸溶液能与硝酸钡等含有钡离子的溶液反应生成硫酸钡白色沉淀,而盐酸不能,因此可以选择硝酸钡(或氯化钡或氢氧化钡)鉴别;
(4)Ca(OH)2+2HCl=CaCl2+2H20; Ca(OH)2+H2SO4=CaSO4 +2H2O可知,氢氧化钙和盐酸反应的质量比是74:73.,而和硫酸反应的质量比为74:98,等质量的氢氧化钙需用的硫酸多,因此硫酸不够把氢氧化钙反应完,剩氢氧化钙,溶液显碱性,pH大于7.
故答案为:(1)酸根离子不同;(2)浓盐酸;(3)硝酸钡(或氯化钡或氢氧化钡);(4)>.
点评 本题难度不是很大,主要考查了酸的有关的化学性质及有关化学方程式的意义,能够考查学生分析问题的能力.


科目:初中化学 来源: 题型:填空题
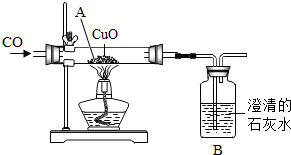 如图为一氧化碳还原氧化铜的装置图.
如图为一氧化碳还原氧化铜的装置图.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶液都是无色透明的 | |
| B. | 饱和溶液不能再溶解任何物质 | |
| C. | 硝酸铵溶解在水中,溶液温度会降低 | |
| D. | 向饱和的石灰水中加入CaO,溶质质量不变 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
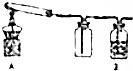 某课外活动小组的同学将过量的炭粉和16克氧化铜均匀混合,用如图所示装置进行实验,图中铁架台等装置已略去;反应一段时间后停止加热,冷却到室温,反应前、后测得的数据如下:
某课外活动小组的同学将过量的炭粉和16克氧化铜均匀混合,用如图所示装置进行实验,图中铁架台等装置已略去;反应一段时间后停止加热,冷却到室温,反应前、后测得的数据如下:| 装置 | 反应前 | 反应后 |
| A | 试管的质量38.2 克 氧化铜和炭粉混合物的质量20.0克 | 试管和固体物质的质量56.8克 |
| B | 反应后瓶内石灰水比反应前增重1.1 克 | |
| A. | 装置中可能还有一部分CO2未被石灰水溶液吸收 | |
| B. | 氯化铜和炭粉反应产生的气体除CO2外还有CO | |
| C. | 氧化铜和炭粉可能没有完全反应 | |
| D. | 该反应不符合质量守恒定律 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 20℃时100克氯化钠溶液中含有36克氯化钠 | |
| B. | 20℃时100克氯化钠饱和溶液中含有36克氯化钠 | |
| C. | 20℃时100克水中达到饱和状态时能溶解36克氯化钠 | |
| D. | 20℃时氯化钠溶液中溶质的质量分数为36% |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com