
| ����ϡ��������/g | 9.6 | 9.8 | 9.9 | 10.0 | 10.1 |
| ��Һ��pH | 12.4 | 12.1 | 11.8 | 7.0 | 2.2 |
���� ��1�����ݵ�����ϡ��������Ϊ9.8gʱ��Һ��pH�ж�Һ�е����ʽ��
��2������ǡ�÷�Ӧʱ���ĵ����������������������Ƶ��������ɽ��
��3�����ݻ�ѧ��Ӧǰ����Ԫ�ص�����������
��� �⣺��1��������ϡ��������Ϊ10.1gʱ����Һ��pH��2.2����Һ�����ԣ���Һ�е��������Ȼ��ƺ��Ȼ��⣬��ѧʽΪ��NaCl��NaOH��
��2����20.0g����������Һ�����ʵ�����Ϊx��
HCl+NaOH�TNaCl+H2O
36.5 40
10g��7.3% x
$\frac{36.5}{10g��7.3%}$=$\frac{40}{x}$
x=0.8g
����������Һ�����ʵ�����������0.8g/20g��100%=4%��
��3�����������غ㶨�ɣ���Ӧǰ��NaԪ�ص��������䣮
����NaԪ�ص�����=0.8g��23/40��100%=0.46g
����������������Һ�����ʵ�����������4%��NaԪ�ص�����=0.8g��23/40��100%=0.46g��
�ʴ�Ϊ����1��NaCl��NaOH��
��2����������������Һ�����ʵ���������4%��
��3��0.46g��
���� ������Ҫ������ѧ�����ݻ�ѧ����ʽ���м�����������漰��Ϊ��϶࣬���ѶȲ��ؼ��ǽ��ⲽ��Ҫ�淶��


 Ӧ������ҵ��ϵ�д�
Ӧ������ҵ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | H2��CO��CO2 | B�� | CO��CO2��H2O������ | C�� | H2��CO2��N2 | D�� | H2��CO��CH4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ��̽����
 ʵ���Ұ���ͼ��ʾװ����ȡCO2��������CO2�����ʣ��Իش��������⣺
ʵ���Ұ���ͼ��ʾװ����ȡCO2��������CO2�����ʣ��Իش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 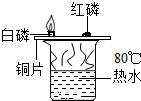 ֤����ȼ��ȼ����Ҫ���� | B�� | 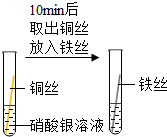 �Ƚ�Fe��Cu��Ag�Ľ������ | ||
| C�� |  ����������Ũ��Ϊ2%��ʯ��ˮ | D�� | 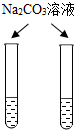 ����ϡ������ϡ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
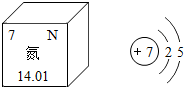 �������ڱ��е���Ϣ��ԭ�ӽṹʾ��ͼ��ͼ��
�������ڱ��е���Ϣ��ԭ�ӽṹʾ��ͼ��ͼ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
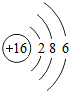 ���ڻ�ѧ��Ӧ���ã���á���ʧ�������ӣ��Ƿǽ�������������ǽ�������Ԫ�أ�
���ڻ�ѧ��Ӧ���ã���á���ʧ�������ӣ��Ƿǽ�������������ǽ�������Ԫ�أ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 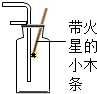 �������� | B�� |  ��Һ����� | C�� |  ����Һ�� | D�� | 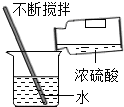 ϡ��Ũ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������̼���⡢������Ԫ����ɵĻ����� | |
| B�� | �����������ͼ�����ɵĻ���� | |
| C�� | ���ķ�����̼���⡢��Ԫ�ص�ԭ�Ӹ�������6��1��35.5 | |
| D�� | �����ɶ���ԭ�ӹ��ɵ�һ�ֻ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com