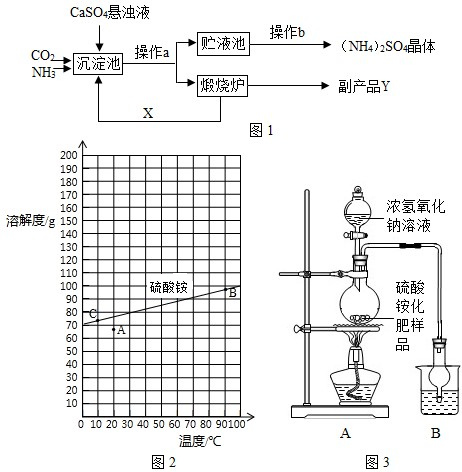
£Ø2011?µ¤ŃōŹŠ¶žÄ££©Ä³ŠĖȤŠ”×éŌŚø“Ļ°ĢśµÄŅ±Į¶Ź±£¬ŌŚ²Īæ¼×ŹĮĻÉĻ·¢ĻÖŅŌĻĀŅ»¶ĪĪÄ×Ö£ŗŅŃÖŖŌŚ²»Ķ¬µÄĪĀ¶ČĻĀ£¬COÓėĢśµÄŃõ»ÆĪļ·“Ó¦ÄÜÉś³ÉĮķŅ»ÖÖĢśµÄŃõ»ÆĪļ£Ø»ņĢśµ„ÖŹ£©ŗĶCO
2£®ĖūĆĒ²»½ū²śÉśĮĖŅÉĪŹ£ŗŹé±¾119Ņ³µÄŹµŃéÖŠ£¬COÓėFe
2O
3·“Ӧɜ³ÉµÄŗŚÉ«ĪļÖŹÕęµÄŹĒFe·ŪĀš£æÓŚŹĒĖūĆĒ½ųŠŠĮĖŅŌĻĀĢ½¾æ£®
”¾²éŌÄ׏ĮĻ”æ
׏ĮĻŅ»£ŗFe·ŪŗĶFe
3O
4·ŪÄ©Äܱ»“ÅĢśĪüŅż¶ųFeO£ØŗŚÉ«£©²»ÄÜ£»
׏ĮĻ¶ž£ŗFe
3O
4ÖŠĢśŌŖĖŲÓŠ+2”¢+3Į½ÖÖ»ÆŗĻ¼Ū£¬Ęä»ÆѧŹ½æÉÓĆFeO?Fe
2O
3 µÄŠĪŹ½±ķŹ¾£»
”¾Ģį³ö²ĀĻė”æŗŚÉ«ĪļÖŹæÉÄÜŹĒFe
3O
4”¢FeOŗĶFe·ŪÖŠµÄŅ»ÖÖ»ņ¼øÖÖ£®
”¾½ųŠŠŹµŃé”æŠĖȤŠ”×éŹÕ¼ÆĮĖCOÓėFe
2O
3·“Ӧɜ³ÉµÄŗŚÉ«ĪļÖŹ½ųŠŠĮĖĻĀĮŠŹµŃé£ŗ
|
ŹµŃé·½°ø |
ŹµŃéĻÖĻó |
| ¼× |
ȔɣĮæŗŚÉ«ĪļÖŹÓĆ“ÅĢśĪüŅż |
ŗŚÉ«ĪļÖŹČ«²æ±»“ÅĢśĪüŅż |
| ŅŅ |
ȔɣĮæŗŚÉ«ĪļÖŹ¼ÓČė30%ČȵÄŃĪĖįÖŠ |
ĪŽĘųÅŻ”¢ČÜŅŗŃÕÉ«±ä³É»ĘĀĢÉ« |
| ±ū |
ȔɣĮæŗŚÉ«ĪļÖŹ¼ÓČėĮņĖįĶČÜŅŗÖŠ |
ĪŽČĪŗĪĻÖĻó |
”¾ŹµŃé½įĀŪ”æ
£Ø1£©¼×ŹµŃéĻÖĻóĖµĆ÷ŗŚÉ«Īļ֏֊ƻӊ
FeO
FeO
£¬ŅŅ”¢±ūŹµŃéĻÖĻóĖµĆ÷ŗŚÉ«Īļ֏֊ƻӊ
Fe
Fe
£»
£Ø2£©Éś³ÉµÄŗŚÉ«ĪļÖŹÓ¦ĪŖFe
3O
4£»
£Ø3£©Š“³öŗŚÉ«·ŪÄ©ŗĶČȵÄŃĪĖį·“Ó¦µÄ»Æѧ·½³ĢŹ½
Fe3O4+8HClØTFeCl2+2FeCl3+4H2O
Fe3O4+8HClØTFeCl2+2FeCl3+4H2O
£»
”¾ĶŲÕ¹Ģ½¾æ”æĶ¬Ń§ĆĒ¶ŌFe
3O
4²śÉśĮĖŠĖȤ£¬“Ó²Īæ¼×ŹĮĻÖŠÕŅµ½ĮĖŃõ»Æ³Įµķ·ØÉś²śø“Ó”ÓĆøßµµFe
3O
4·ŪµÄ¹¤ŅÕĮ÷³Ģ¼ņĶ¼£®
”¾Éś²śĮ÷³Ģ”æ
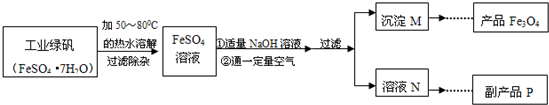
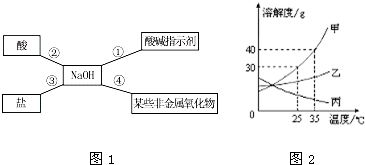
”¾²éŌÄ׏ĮĻ”æ
׏ĮĻŅ»£ŗĮņĖįŃĒĢśŌŚ²»Ķ¬ĪĀ¶ČĻĀµÄČܽā¶ČČēĻĀ±ķĖłŹ¾£ŗ
| ĪĀ¶Č/”ę |
0 |
10 |
30 |
50 |
60 |
70 |
80 |
90 |
| Čܽā¶Č/g |
14.0 |
17.0 |
25.0 |
33.0 |
35.3 |
33.0 |
30.5 |
27.0 |
׏ĮĻ¶ž£ŗFe£ØOH£©
2ŹÜŃõĘųŃõ»Æ·“Ó¦ŌĄķĪŖ£ŗ4Fe£ØOH£©
2+2H
2O+O
2=4Fe£ØOH£©
3׏ĮĻČż£ŗ»ńµĆFe
3O
4µÄ·“Ó¦ŌĄķĪŖ£ŗFe£ØOH£©
2+2Fe£ØOH£©
3Fe
3O
4+4H
2O
”¾ĪŹĢāĢÖĀŪ”æ
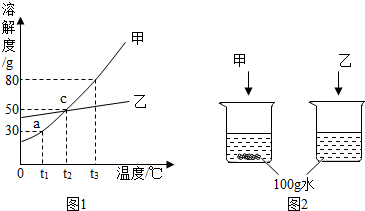
£Ø1£©ČܽāŹ±£¬ÓĆ50”ęÖĮ80”ęµÄČČĖ®ÄæµÄŹĒ
ŌŚ50”ꔫ80”ꏱ£¬ĮņĖįŃĒĢśµÄČܽā¶Č½Ļ“ó£¬ÓŠĄūÓŚČܽāµÄøü¶ą£¬Ģįøß²śĀŹ
ŌŚ50”ꔫ80”ꏱ£¬ĮņĖįŃĒĢśµÄČܽā¶Č½Ļ“ó£¬ÓŠĄūÓŚČܽāµÄøü¶ą£¬Ģįøß²śĀŹ
£®
£Ø2£©Š“³ö¼ÓČėŹŹĮæNaOHČÜŅŗŹ±·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½
2NaOH+FeSO4ØTFe£ØOH£©2”ż+Na2SO4
2NaOH+FeSO4ØTFe£ØOH£©2”ż+Na2SO4
£»
£Ø3£©ÉĻŹö¹ż³ĢÖŠ£¬ŅŖæŲÖĘ”°ĶØŅ»¶ØĮææÕĘų”±µÄÄæµÄŹĒ
æŲÖĘFe£ØOH£©2×Ŗ»ÆĪŖFe£ØOH£©3µÄĮæ[»ņ·ĄÖ¹Fe£ØOH£©2ĶźČ«×Ŗ»ÆĪŖFe£ØOH£©3]
æŲÖĘFe£ØOH£©2×Ŗ»ÆĪŖFe£ØOH£©3µÄĮæ[»ņ·ĄÖ¹Fe£ØOH£©2ĶźČ«×Ŗ»ÆĪŖFe£ØOH£©3]
£®
£Ø4£©ŅŖŹ¹ĖÄŃõ»ÆČżĢśµÄ²śĀŹ×īøߣ¬ŌņÉĻŹöĮ÷³ĢÖŠ²śÉśµÄFe£ØOH£©
2ŗĶFe£ØOH£©
3µÄ×ī¼ŃÖŹĮæ±ČĪŖ
90£ŗ214£Ø»ņ45£ŗ107£©
90£ŗ214£Ø»ņ45£ŗ107£©
£®
£Ø5£©ø±²śĘ·PŹĒĮņĖįÄĘ£¬ÓÉČÜŅŗN»ńµĆøĆø±²śĘ·µÄ²Ł×÷Ė³ŠņŹĒb”ś
c
c
”ś
a
a
”śd£®
a£®¹żĀĖ b£®¼ÓČČÅØĖõ c£®ĄäČ“½į¾§ d£®¾§Ģå¼ÓČČÖĮĶźČ«Ź§Č„½į¾§Ė®
”¾×é³ÉČ·¶Ø”æĪŖČ·¶ØÓĆŅŌÉĻ·½·ØÖʵƵÄĖÄŃõ»ÆČżĢśÖŠæÉÄÜŗ¬ÓŠµÄŌÓÖŹ£¬Ķ¬Ń§ĆĒÓÖ½ųŠŠĮĖĻĀĮŠŹµŃéĢ½¾æ£®
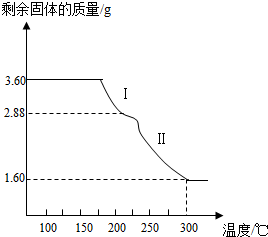
”¾²éŌÄ׏ĮĻ”æ
׏ĮĻŅ»£ŗÄŃČÜŠŌ¼īŹÜČČŹ±ÄÜ·Ö½ā²śÉś½šŹōŃõ»ÆĪļŗĶĖ®£Ø·“Ó¦ÖŠø÷ÖÖŌŖĖŲµÄ»ÆŗĻ¼Ū²»±ä£©£»
׏ĮĻ¶ž£ŗFe
2O
3ŗĶCO·“Ó¦ŹĒĖęĪĀ¶ČÉżø߶ųÖš²½½ųŠŠµÄ£¬ĻČÉś³ÉFe
3O
4£¬ŌŁÉś³ÉFeO£ØŗŚÉ«£©£¬×īŗóÉś³ÉFe£»
”¾Ģį³ö²ĀĻė”æFe
3O
4ÖŠæÉÄÜŗ¬ÓŠµÄŌÓÖŹŹĒFe
2O
3ŗĶFeOÖŠµÄŅ»ÖÖ»ņĮ½ÖÖ£®
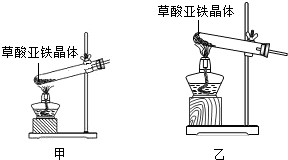
”¾ŹµŃéÉč¼Ę”æĶ¬Ń§ĆĒ³ĘČ”ĮĖ23.28gøĆFe
3O
4ѳʷ½ųŠŠĮĖĻĀĮŠŹµŃé£ŗ
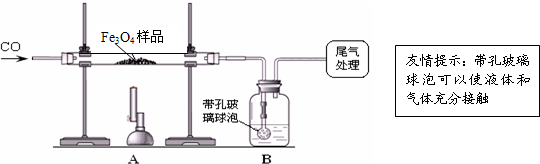
”¾ŹµŃé·ÖĪö”æŅņĢ½¾æĖ¼Ā·²»Ķ¬£¬ŠĖȤŠ”×é·Ö³É¼×”¢ŅŅĮ½Š”×飮
¼××é£ŗ
£Ø1£©øĆ×éĶ¬Ń§ÓūĶعżB×°ÖĆ·“Ó¦Ē°ŗóµÄÖŹĮæ±ä»ÆĄ“¼ĘĖćČ·ČĻøĆFe
3O
4ѳʷ֊µÄŌÓÖŹ£®BÖŠµÄ×ī¼ŃŹŌ¼ĮŹĒ_
¢Ś
¢Ś
£ØĢīŠņŗÅ£©£®
¢Ł³ĪĒåŹÆ»ŅĖ® ¢ŚĒāŃõ»ÆÄĘÅØČÜŅŗ ¢ŪĻ”ŃĪĖį ¢ÜĖ®
£Ø2£©ÉĻŹöŹµŃé¹ż³ĢÖŠ£¬COĘųĢå³ż×÷ĪŖ·“Ó¦ĪļĶā£¬»¹ÄÜĘšµ½µÄ×÷ÓĆŹĒ£ŗ¢ŁŹµŃéæŖŹ¼Ź±£¬Åž”×°ÖĆÖŠµÄæÕĘų£¬·ĄÖ¹¼ÓČČŹ±·¢Éś±¬ÕØ£»¢ŚĶ£Ö¹¼ÓČČŗ󣬷ĄÖ¹AÖŠÉś³ÉĪļ±»Ńõ»Æ£¬BÖŠµÄČÜŅŗµ¹ĪüČėAÖŠ£»¢Ū
½«×°ÖĆÖŠµÄCO2ĖĶČėNaOHČÜŅŗÖŠ
½«×°ÖĆÖŠµÄCO2ĖĶČėNaOHČÜŅŗÖŠ
£®
£Ø3£©ŅŅ×éĶ¬Ń§ČĻĪŖB×°ÖĆ·“Ó¦Ē°ŗóµÄ
ÖŹĮæ²ī»įĘ«Š”¶ųÓ°Ļģ¼ĘĖć”¢·ÖĪö£¬ÄćČĻĪŖĖūĆĒµÄĄķÓÉŹĒ
CO“ÓBÖŠČÜŅŗĄļŅŻ³öŹ±»į“ų³ö²æ·ÖĖ®ÕōĘų
CO“ÓBÖŠČÜŅŗĄļŅŻ³öŹ±»į“ų³ö²æ·ÖĖ®ÕōĘų
£®
ŅŅ×é£ŗ
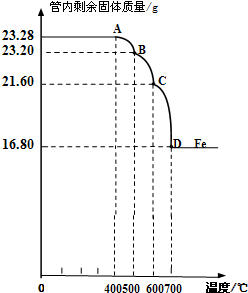
ĄūÓĆŅĒĘ÷²ā¶Ø²¢»ęÖĘ³É·“Ó¦¹ż³ĢÖŠA×°ÖĆÖŠ²£Į§¹ÜÄŚµÄ¹ĢĢåÖŹĮæĖęĪĀ¶ČµÄ±ä»ÆĒśĻߣØÓŅĶ¼£©£®
£Ø1£©Š“³öBC¶Ī·¢Éś·“Ó¦µÄ»Æѧ·½³ĢŹ½£ŗ
£®
£Ø2£©Ķعż¼ĘĖćČ·¶Ø£ŗøĆFe
3O
4ѳʷ֊ŗ¬ÓŠµÄŌÓÖŹŹĒ
Fe2O3
Fe2O3
£¬ĘäÖŠŗ¬Fe
3O
4µÄÖŹĮæŹĒ
20.88
20.88
g£®£Ø²»ŠčŅŖŠ“¹ż³Ģ£©

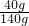 ”Į100%=28.6%
”Į100%=28.6%

 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø


 ÖŹĮæ²ī»įĘ«Š”¶ųÓ°Ļģ¼ĘĖć”¢·ÖĪö£¬ÄćČĻĪŖĖūĆĒµÄĄķÓÉŹĒ
ÖŹĮæ²ī»įĘ«Š”¶ųÓ°Ļģ¼ĘĖć”¢·ÖĪö£¬ÄćČĻĪŖĖūĆĒµÄĄķÓÉŹĒ