
| 选项 | 物质 | 所含杂质 | 除去杂质的方法 |
| A | 硝酸钾 | 少量氯化钠 | 重结晶 |
| B | N2 | O2 | 通过灼热的铜网 |
| C | CaCl2溶液 | 稀盐酸 | 加入过量碳酸钙,过滤 |
| D | Fe | 铁锈 | 稀硫酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、KNO3和NaCl的溶解度受温度的影响不同,硝酸钾溶解度受温度影响较大,而氯化钠受温度影响较小,所以可采取加热水溶解配成饱和溶液、冷却热饱和溶液使KNO3先结晶出来、再过滤的方法;用重结晶的方法可以除去杂质;故选项所采取的方法正确.
B、氧气通过灼热的铜网时可与铜发生反应生成氧化铜,而氮气不与铜反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
C、稀盐酸能与过量的碳酸钙反应生成氯化钙、水和二氧化碳,再过滤除去过量的碳酸钙,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、铁锈的主要成分是氧化铁,能与适量的稀硫酸反应生成硫酸铁和水,但若稀硫酸过量,会与铁反应,不符合除杂原则,故选项所采取的试剂错误.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:初中化学 来源: 题型:选择题
| A.化学反应基本类型 | B.化学反应中常见的“三” |
| ①化合反应:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5 ②分解反应:H2CO3═H2O+CO2↑ ③置换反应:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+CO2 | ①煤、石油、天然气-三大化石燃料 ②塑料、合成纤维、合成橡胶-三大合成材料 ③分子、原子、离子-构成物质的三种粒子 |
| C.对鉴别方法的认识 | D.化学与生活 |
| ①区分氮气和氧气-伸入带火星的木条 ②区分棉纤维和羊毛纤维-点燃后闻气味 ③区分硫酸铵和氯化铵-加熟石灰粉末研磨 | ①用甲醛水溶液浸泡水产品防腐 ②缺乏维生素C易患坏血病 ③自行车支架喷油漆防锈 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氧气具有可燃性,可用于炼钢、航天 | |
| B. | 金刚石是天然存在最硬的物质,可用于切割大理石 | |
| C. | 钛的合金与人体“相容性”好,可用于制造人造骨 | |
| D. | 浓硫酸具有吸水性,实验室可用作干燥剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
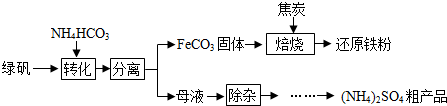
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
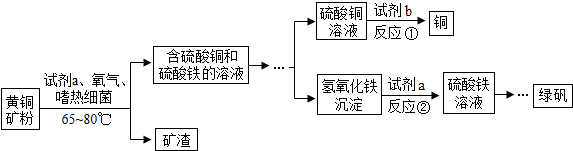
| A. | 分离出矿渣的操作是过滤 | B. | 试剂a是硫酸溶液 | ||
| C. | 反应②是复分解反应 | D. | 试剂b只能是铁粉 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
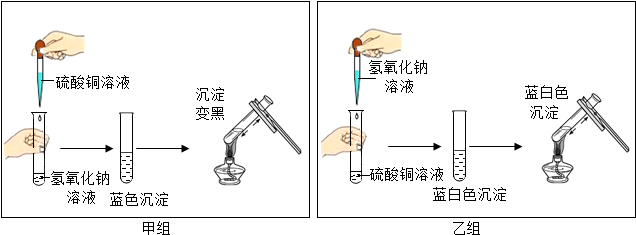
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com