
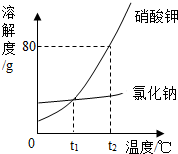
 如图是氯化钠与硝酸钾的溶解度曲线,回答:
如图是氯化钠与硝酸钾的溶解度曲线,回答:分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)配置200g0.9%的医用生理盐水,需要NaCl的质量为200g×0.9%=1.8g;
(2)由图可知,t1℃时,硝酸钾的溶解度=氯化钠的溶解度;欲提纯混有少量氯化钠的硝酸钾固体,应采用的方法是降温结晶,在农业上硝酸钾可作氮肥;
(3)t2℃时,硝酸钾的溶解度是80g,所以将50g硝酸钾固体完全溶于50g水,形成溶液的质量是90g,该硝酸钾溶液中含有的阴离子是N${{O}_{3}}^{-}$.
故答案为:(1)1.8g;
(2)=,降温结晶,氮;
(3)90,N${{O}_{3}}^{-}$.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


科目:初中化学 来源: 题型:实验探究题
| 名称 | 分子式 | 颜色、状态 | 溶解性 | 熔点(℃) | 密度(g/cm3) |
| 草酸 | H2C2O4 | - | 易溶于水 | 189.5 | 1.900 |
| 草酸晶体 | H2C2O4•2H2O | 无色晶体 | -[ | 101.5 | 1.650 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 取滤液于试管中滴加足量的硝酸钙溶液,再滴入几滴酚酞试液 | 出现白色沉淀,酚酞试液变红色 | 猜想正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取滤液于试管中滴加少量的稀盐酸 | 无明显现象 | 猜想正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
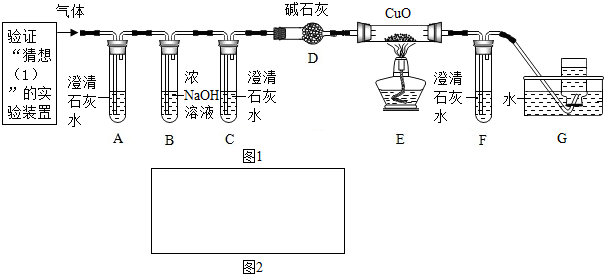
 过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解成氧气和水.分液漏斗可以通过调节活塞控制液体滴加速度.回答下列问题:
过氧化氢溶液在二氧化锰作催化剂的条件下能迅速分解成氧气和水.分液漏斗可以通过调节活塞控制液体滴加速度.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 序号 | 加入稀盐酸的质量/g | 剩余固体质量/g |
| 第一次 | 10 | 5.5 |
| 第二次 | 10 | m |
| 第三次 | 10 | 1.2 |
| 第四次 | 10 | 1.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 氧化还原反应是指反应前后元素的化合价发生变化的反应.如图概括了四种基本反应类型与氧化还原反应的关系,下列反应所在图示位置的说法错误的是( )
氧化还原反应是指反应前后元素的化合价发生变化的反应.如图概括了四种基本反应类型与氧化还原反应的关系,下列反应所在图示位置的说法错误的是( )| A. | Ca(OH)2+Na2CO3═CaCO3↓+2NaOH可放在①位置 | |
| B. | 实验室制取氢气的反应以及铁和硫酸铜溶液的反应可放在③位置 | |
| C. | CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑和水分解的反应可放在②位置 | |
| D. | 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2是氧化还原反应可放在③位置 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 质子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 元素 名称 | ||||||||||
| 元素 符号 | ||||||||||
| 质子数 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
| 元素 名称 | ||||||||||
| 元素 符号 | ||||||||||
| 元素 名称 | 锰 | 铁 | 铜 | 锌 | 钡 | 汞 | 银 | 金 | 铬 | 镍 |
| 元素 符号 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 化肥对提高农作物的产量具有重要作用,应提倡大量使用 | |
| B. | 农作物生长时出现枝叶泛黄、植株瘦小应多施钾肥 | |
| C. | Ca3(PO4)2属于复合肥料 | |
| D. | 通过观察外观来区别氮肥和磷肥 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com