
| 酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
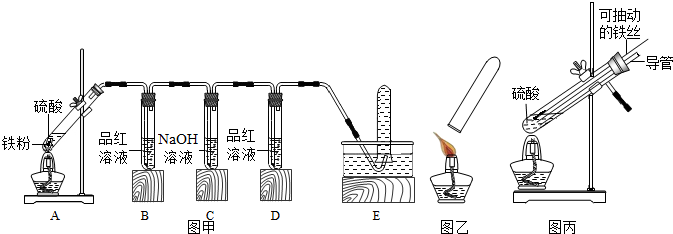
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有SO2和H2 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
分析 根据实验现象可以判断实验结论,根据实验结论可以判断实验现象;
铁和稀硫酸反应生成硫酸亚铁和氢气;
氢气燃烧生成水;
氢氧化钠溶液能够吸收二氧化硫,并且氢氧化钠和二氧化硫反应生成亚硫酸钠和水;
不同的实验装置,功能不同.
解答 解:【实验探究】完成实验如下表所示:
| A中硫酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有SO2和H2 |
实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
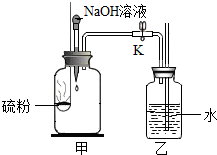 实验小组用如图所示装置进行实验.已知:2NaOH+SO2═Na2SO3+H2O
实验小组用如图所示装置进行实验.已知:2NaOH+SO2═Na2SO3+H2O| A. | ①中,硫燃烧呈淡蓝色火焰 | |
| B. | ②中,甲装置内的气压减小,最终与大气压相等 | |
| C. | ③中,乙中的长导管口处冒气泡 | |
| D. | 甲装置中硫粉换做碳粉,则乙中长导管口可能冒出气泡很少 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. |  探究质量守恒定律 | |
| B. |  探究Mg、Fe、Cu的金属活动性 | |
| C. | 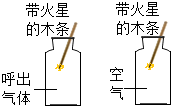 探究呼出气体和空气中氧气含量的不同 | |
| D. | 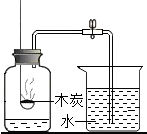 测定空气里氧气 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | HCl、(NH4)2SO4、Ba(OH)2、Na2SO4 | B. | CuSO4、KOH、NaCl、NaOH | ||
| C. | Na2CO3、Na2SO4、BaCl2、HNO3 | D. | NaOH、Na2CO3、酚酞、CaCl2 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | AgS | B. | Ag2S | C. | Ag2O2 | D. | Ag2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1:2 | B. | 1:1 | C. | 32:1 | D. | 4:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com