
| 温度t/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
| 溶解度S/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 |
| 析出晶体 | FeSO4•7H2O | FeSO4•4H2O | FeSO4•H2O | |||||||
分析 根据已有的铁的性质、铁的冶炼方法、以及根据化学方程式的计算进行分析解答即可.
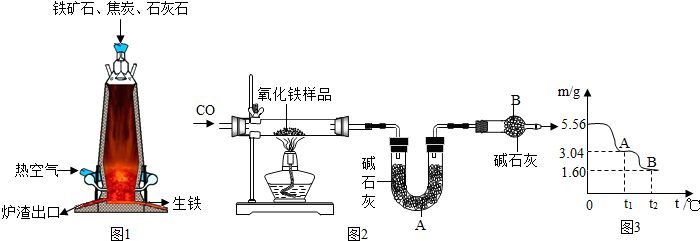
解答 解:(1)从炉底流出的生铁是铁和碳的混合物,属于铁的合金;在高炉炼铁中碳能燃烧产生热量、能生成一氧化碳作为还原氧化铁的物质,故填:合金,D;
(2)【问题讨论】装置B中盛有的是碱石灰,碱石灰能吸收空气中的水和二氧化碳,防止对实验结果造成干扰,一氧化碳是有毒的气体,而该装置中没有进行尾气处理,故填:吸收空气中的水和二氧化碳;未进行尾气处理;
【数据处理】称取样品8.0g,用上述装置进行实验,充分反应后称量A装置增重4.4g.说明生成二氧化碳的质量为4.4g,设氧化铁的质量为x
Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
160 132
x 4.4g
$\frac{160}{132}=\frac{x}{4.4g}$
x≈5.3g
则样品中氧化铁质量分数为$\frac{5.3g}{8g}×100%$=66.3%,故填:66.3.
【实验反思】当观察到反应管中固体全部变黑后,若立即停止通CO,装置A增重不变,测得的样品中氧化铁的质量分数无影响,故填:无影响;
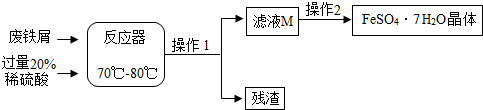
(3)①通过分析可知,铁和硫酸反应生成了硫酸亚铁和氢气,氧化铁和硫酸反应生成了硫酸铁和水,铁与硫酸铁反应生成硫酸亚铁.故填:Fe+H2SO4═FeSO4+H2↑;
②加入的硫酸是过量的,所以在溶液中含有硫酸和反应生成的硫酸亚铁,所以滤液M中肯定含有的溶质的化学式是:FeSO4、H2SO4;操作2后得到了滤液和固体,所以可以判断操作2为过滤,故填:FeSO4、H2SO4;过滤;
③根据图表中的信息可以知道当温度大于60℃时产生了FeSO4•4H2O,所以应该将温度控制在60℃以下;故填:60.
(4)5.56g硫酸亚铁晶体(FeSO4•xH2O)隔绝空气受热分解时,生成金属氧化物和气体.固体产物的质量随温度变化的曲线如图所示.
①0-t1℃,发生的变化是加热失去结晶水,
FeSO4•xH2O$\frac{\underline{\;\;△\;\;}}{\;}$FeSO4+xH2O
152+18x 152
5.56g 3.04g
$\frac{152+18x}{152}=\frac{5.56g}{3.04g}$
x=7;
故填:7;
②硫酸亚铁分解生成金属氧化物和气体,t2℃时B点固体组成只有一种,故是氧化铁,故填:Fe2O3.
点评 本题考查的是金属的有关性质的知识,完成此题,可以依据已有的知识结合题干提供的信息进行.


 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案科目:初中化学 来源: 题型:选择题
| A. | MnO2(KCl)加水溶解、过滤、蒸发、结晶 | |
| B. | KCl(K2CO3)加足量稀硫酸、过滤、蒸发、结晶 | |
| C. | CuO(Cu)加足量稀盐酸、过滤、洗涤、干燥 | |
| D. | BaSO4(BaCO3)加足量稀盐酸、过滤、洗涤、干燥 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

| 实验操作 | 实验现象 | 实验结论 |
| 将步骤三B试管中溶液倒入盛有锌粒的试管中 | 有气泡产生 | 猜想一正确 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 可知在化学反应中,镁原子易失去(选填“得到”或“失去”)电子形成镁离子,其离子符号表示为:Mg2+.
可知在化学反应中,镁原子易失去(选填“得到”或“失去”)电子形成镁离子,其离子符号表示为:Mg2+.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO2气体(CO)→点燃 | |
| B. | MnO2固体(KCl)→加水溶解,过滤,洗涤,干燥 | |
| C. | CO2气体(HCl)→通入NaOH溶液中 | |
| D. | KCl溶液(K2CO3)→加稀H2SO4 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原溶液可能饱和也可能不饱和 | |
| B. | 析出晶体后的溶液可能是饱和溶液也可能是不饱和溶液 | |
| C. | 析出晶体后的溶液可能是浓溶液,也可能是稀溶液 | |
| D. | 再降温不一定会有晶体析出 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com