
【题目】碳酸钠和碳酸氢钠是生活中常见的盐,课外小组通过以下实验进行鉴别。
实验1
实验序号 实验操作 | 1-1碳酸钠 | 1-2碳酸氢钠 |
| 11.96 | 8.28 |
实验2
实验序号 实验操作 | 2-1碳酸钠溶液 | 2-2碳酸氢钠溶液 |
|
| |
实验3
实验序号 实验操作 | 3-1碳酸钠溶液 | 3-2碳酸氢钠溶液 |
| 不分解 | 2NaHCO3△ Na2CO3 +CO2 ↑+H2O |
回答下列问题:
(1)实验1中控制的变量是__________,实验1得出的结论是__________。
(2)实验2的目的是__________。
(3) ①实验3-2中观察到的现象是__________。
②完全分解8.4gNaHCO3能生成CO2__________g。
③要确定碳酸氢钠的分解产物,还需进行的实验是__________。
【答案】 温度、溶液浓度; 室温下,10%的碳酸钠溶液的碱性大于碳酸氢钠溶液 1%的盐酸与2%的碳酸钠、碳酸氢钠溶液反应速率是否相同 澄清石灰水变浑浊,试管内壁有液滴 2.2 取完全反应后的剩余固体于试管中,滴加稀盐酸,并将产生的气体通入澄清石灰水
【解析】碳酸钠和碳酸氢钠是生活中常见的盐,溶液均呈碱性,与盐酸反应均可产生二氧化碳气体。(1)实验1中控制的变量是温度、溶液浓度,实验1得出的结论是室温下,10%的碳酸钠溶液的碱性大于碳酸氢钠溶液;pH>7溶液呈碱性,pH<7溶液呈酸性,pH值越大,碱性越强,酸性越弱。(2)实验2的目的是1%的盐酸与2%的碳酸钠、碳酸氢钠溶液反应速率是否相同。(3) ①实验3-2中观察到的现象是澄清石灰水变浑浊,试管内壁有液滴,碳酸氢钠加热分解生成碳酸钠,水和二氧化碳。②完全分解8.4gNaHCO3能生成CO2 质量∶2NaHCO3![]() Na2CO3 + H2O + CO2↑,2NaHCO3 →CO2,168→44,
Na2CO3 + H2O + CO2↑,2NaHCO3 →CO2,168→44,![]() =
=![]() ,x=2.2g。③要确定碳酸氢钠的分解产物,还需进行的实验是取完全反应后的剩余固体于试管中,滴加稀盐酸,并将产生的气体通入澄清石灰水。
,x=2.2g。③要确定碳酸氢钠的分解产物,还需进行的实验是取完全反应后的剩余固体于试管中,滴加稀盐酸,并将产生的气体通入澄清石灰水。
点睛∶同种温度,相同浓度的碳酸钠溶液的碱性大于碳酸氢钠溶液的碱性。 鉴别碳酸钠和碳酸氢钠,可以通过测定其碱性大小,也可以通过与稀盐酸反应速率快慢。


科目:初中化学 来源: 题型:
【题目】有一包粉末,已知由BaSO4、FeCl3、Ba(NO3)2、Na2SO4、NaOH、NaCl中的几种组成。为了确定其成分,现进行以下实验,各步骤均已充分反应。
步骤一:取一定质量的粉末,加水搅拌后过滤,得到有色沉淀甲和无色溶液A;
步骤二:向步骤一的沉淀甲中加入足量稀盐酸,固体全部消失并得到黄色溶液;
步骤三:将步骤一得到的无色溶液A进行如下图所示的实验。

则下列说法中正确的是:
A. 原白色粉末中一定有FeCl3、Na2SO4、NaOH
B. 有色沉淀甲可能是Fe(OH)3和BaSO4 的混合物
C. 若将步骤二中的盐酸换成硝酸,则可确定原白色粉末是否含有NaCl
D. 原白色粉末中FeCl3和NaOH的质量比为65:48
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用化学用语填空。
(1)氦气______________,(2)2个氮分子______________,
(3)3个铵根离子___________,(4)氧化铁中铁的化合价______________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知物质A~H为初中化学常见物质,请根据下列表述回答问题。
(1)已知A、B、C、D均含有两种元素,且物质B、D元素组成相同。固体A中加入液体B,能放出大量热。将固体C加入D的水溶液中,有气泡产生,充分反应后过滤,只得到液体B和固体C.
①A跟B反应的生成物可用于改良酸性土壤或用于建筑材料等,则A和B反应的化学方程式为_________.
②C的化学式为______________.
(2)固体E、F和物质G、H的水溶液中,任意一种固体与任意一种溶液混合均有气泡产生。E通过其他反应途径能生成F。
①若E为单质,E、F的化学式可能为______________ (写一组即可)。
②若E和F均含三种元素,E生成F的化学方程式为:_____________,固体E和二氧化硅在高温条件下可生成硅酸钠(Na2SiO3)和一种能产生温室效应的常见气体,该反应的化学方程式为:__________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】食用油脂能供给人体必需脂肪酸,促进脂溶性维生素的吸收,是最常用的食品和调味品。食用油脂是一种高热量食品,每克油脂在体内氧化释放37.7kJ的热量,比等质量的糖和蛋白质高一倍多,再加上不同油脂成分的差异性,使如何选择和使用食用油脂存在不少盲区和误区。
食用油脂中99%以上是脂肪酸,还含有维生素A、E,少量矿物元素钙、钾等。食用油中脂肪酸种类繁多,主要分类方法见表1。不同油脂中,各种脂肪酸的含量不同,常见食用油中脂肪酸组成(%)如表2。


脂肪酸不仅种类繁多,功能也各异。饱和脂肪酸能平衡血浆中脂肪酸浓度,摄入过高会导致胆固醇、甘油三酯等升高,继而引发动脉管腔狭窄;单不饱和脂肪酸分子内的碳原子之间存在一个碳碳双键(C=C),主要是油酸(C18H34O2,ω-9),油酸能降低总胆固醇和有害胆固醇,但不会降低有益胆固醇;多不饱和脂肪酸主要有亚油酸(C18H32O2,ω-6)和α-亚麻酸(C18H30O2,ω-3),它们是人体必需脂肪酸,而且人体不能合成,必需从食物中摄入。亚油酸有“血管清道夫”的美誉,能防止血清胆固醇在血管壁沉积;α-亚麻酸在人体分解后形成生命活性因子DHA和EPA,是大脑的重要营养要素,DHA能提高记忆力和思维能力,EPA能降低血液中胆固醇和甘油三酯的含量,降低血液粘稠度。
天然状态下,不饱和脂肪酸多数为顺式脂肪酸。反式脂肪酸主要存在于奶油类、煎炸类和烘烤类食品中,受加热过程影响,油品中反式脂肪酸含量(质量分数/%)发生变化。其变化过程如右图所示。反式脂肪酸可妨碍必需脂肪酸在人体内的代谢,提高总胆固醇与高密度脂蛋白的比例,从而增加冠心病发病风险。
依据文中内容,回答下列问题:
(1)食用油脂能为人体提供的营养素有__________。
(2)按油脂分类,花生油属于___________。
(3)常见食用油中多不饱和脂肪酸含量最高的是__________。
(4)关于食用油脂,下列说法正确的是__________。
A.应少吃油炸、烘焙类食品
B.食物营养素中,热量最高的是脂肪
C.烹调食物时,最好将油温控制在260oC以下
D.油酸和亚油酸分子中碳碳双键的个数不同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】高纯氧化铁可作现代电子工业的材料,以下是用硫铁矿烧渣(主要成分为Fe2O3、FeO、SiO2)为原料制备高纯氧化铁(Fe2O3)的生产流程示意图:

已知:(NH4)2CO3溶液呈碱性,40℃以上时(NH4)2CO3分解。
(1)高温时硫铁矿烧渣中的Fe2O3与CO发生反应的化学方程式为______________________________。
(2)实验室中,步骤1、步骤Ⅱ中实现固液分离的操作为________,用到的玻璃仪器有玻璃棒、烧杯、_____等。
(3)步骤Ⅱ中由(NH4)2CO3生成FeCO3的变化属于______________(填基本反应类型),加适量氨水的目的是___________________________________。
(4)洗涤FeCO3的目的是除去表面附着的杂质,洗涤干净的标志是“取最后一次洗涤液,加入适量的________溶液,无白色沉淀产生”。
(5)加入(NH4)2CO3后,该反应必须控制的条件是____________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是某反应的微观示意图,已知:2个甲分子反应生成1个丙分子和3个乙分子,则下列关于该反应的判断正确的是

A. 该反应不遵守质量守恒定律
B. 反应前后无元素化合价改变
C. 该化学反应中分子的数目、种类均发生改变
D. 乙物质属于化合物
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】金属锈蚀是一个世界性难题。
(1)铁生锈是在空气和____共同作用的结果,铁锈中金属阳离子的化学式为____。
(2)金属铝表面常有一层致密的氧化膜,该氧化膜的化学式是_________ 。
(3)为了防止水龙头生锈,其表面常镀一层铬,其防锈的原理是____。
(4)要除去 24 g 铁锈(Fe2O3)至少需要含硫酸多少克的稀硫酸溶液_______。
查看答案和解析>>
科目:初中化学 来源: 题型:
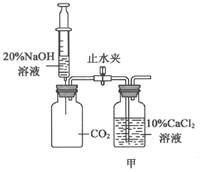
【题目】小金通过图示装置验证CO2能与NaOH发生化学反应。推注射器活塞向充满CO2的集气瓶中注入过量20%的NaOH溶液,振荡集气瓶后打开止水夹。
(1)打开止水夹后观察到的现象是_________。
(2)反应后将集气瓶中混合物过滤,所得溶液中除CaCl2外,还存在的溶质有_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com