

分析 (1)根据质量守恒定律可知,装置和药品的总质量在反应中减少的质量,就是生成氧气的质量,由氧气的质量依据过氧化氢分解的化学方程式可以计算出双氧水溶液中过氧化氢的质量分数进行分析;
(2)根据只有保证氧气中不含其它物质,才能减小误差进行分析.
解答 解:(1)由质量守恒定律可知:反应后生成氧气的质量为:20g+75g+0.5g-95.1g=0.4g,
设双氧水溶液中过氧化氢的质量分数为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
20g×x 0.4g
$\frac{68}{20g×x}$=$\frac{32}{0.4g}$
x=4.25%
(2)用小海设计的装置收集到的氧气中含有少量的水蒸气,使计算出的氧气的质量变大,从而会造成误差.
故答案为:(1)4.25%;
(2)氧气会带走水蒸气.
点评 本题主要考查质量守恒定律的应用、化学方程式的计算、减小误差的措施和仪器的选择,难度稍大,综合性较强.


 第1卷单元月考期中期末系列答案
第1卷单元月考期中期末系列答案科目:初中化学 来源: 题型:选择题
| A. | 二氧化硫 | B. | 氢气 | C. | 二氧化碳 | D. | 一氧化碳 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
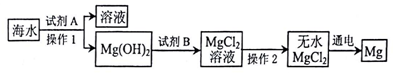
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
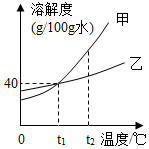 甲、乙两种固体均不含结晶水,在水中不发生反应且溶解性互不影响,它们的溶解度曲线如图所示.下列说法正确的是( )
甲、乙两种固体均不含结晶水,在水中不发生反应且溶解性互不影响,它们的溶解度曲线如图所示.下列说法正确的是( )| A. | t1℃甲、乙的饱和溶液,降低温度,甲先析出晶体 | |
| B. | t1℃时,70g甲的饱和溶液加入40g乙物质,溶液质量仍为70g | |
| C. | 将t2℃甲、乙的饱和溶液分别降温至t1℃,析出晶体的质量:甲>乙 | |
| D. | 将t2℃等质量的甲、乙饱和溶液分别降温至t1℃,析出晶体的质量:甲>乙 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
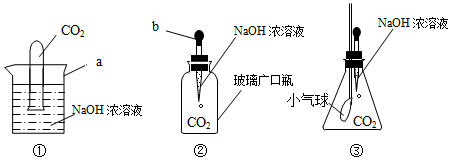
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com