【答案】
分析:(1)微观粒子的特征:质量和体积都很小;微粒与微粒之间有间隙;都是不断运动的.在化学变化中分子可分,原子不可分.水通电分解生成氢气和氧气说明在化学变化中水分子分解成氢原子和氧原子,2个氢原子结合成1个氢分子,2 个氧原子结合成1个氧分子.
(2)过滤可以除去不溶于水的物质;加热煮沸可以降低水的硬度.
(3)根据生活经验和体会回答此问题.
(4)干燥剂的主要成份是生石灰(CaO),吸收水分后生成氢氧化钙Ca(OH)
2,据此写出化学方程式;
(5)利用电解水的方程式根据生成氢气的质量可求反应的水的质量.电解水时硫酸的量不变,分别求出溶质与溶液的质量后进行计算即可.
解答:解:(1)水加热蒸发变成水蒸气是因为水分子之间的间隔随着温度的升高而增大.故填:是因为水分子之间的间隔随着温度的升高而增大;水通电分解生成氢气和氧气说明在化学变化中分子可分,原子不可分.故填:说明在化学变化中分子可分,原子不可分.
(2)过滤可以除去不溶于水的物加,热煮沸可以降低水的硬度.故填:加热煮沸.
(3)根据生活中造成水污染的原因,和浪费水的情况,可考虑以下几点:①回收废旧电池;②洗衣水冲洗厕所;③用洗澡水浇花;等.
(4)这包干燥剂吸收水分的反应方程式是:CaO+H
2O=Ca(OH)
2;
(5)解:利用水电解的方程式,0.6g氢气为已知量求的是反应物物水的质量.
设生成0.6g氢气需要水的质量为x
2H
2O

2H
2↑+O
2↑
36 4
X 0.6g
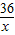
=

x=5.4g
答:生成0.6g氢气需要水的质量为5.4g.
电解水时硫酸的量没有变化,其质量为10g×9.8%=9.8g,溶液的质量是54.4g-5.4g=49g
电解5.4g水后,所得溶液中溶质的质量分数是:

×100%=20%
答:所得溶液中溶质的质量分数是20%
点评:解答本题的关键是要掌握微观粒子的特征和化学变化中分子和原子的关系方面的知识,只有这样才能对问题做出正确的判断;要充分理解净化水的方法方面的知识,只有这样才能对相关方面的问题做出正确的判断.了解水污染现状,增强保护水资源的意识,学会节约用水和防治水污染的方法,是化学学习的重点,也是化学考查的热点.此题还考查学生对氧化钙和氢氧化钙的性质的认识.此题也是对化学方程式计算的考查,主要涉及已知反应物求生成物的计算,属基础性知识考查题.

 2H2↑+O2↑
2H2↑+O2↑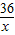 =
=
 ×100%=20%
×100%=20%

 中考解读考点精练系列答案
中考解读考点精练系列答案