
分析 (1)根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
(2)鉴别物质时,首先对需要鉴别的物质的性质进行对比分析找出特性,再根据性质的不同,选择适当的试剂,出现不同的现象的才能鉴别.
解答 解:(1)①CaCO3固体高温煅烧生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.
②CO2能与氢氧化钠溶液反应生成碳酸钠和水,CO不与氢氧化钠溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CO2+2NaOH═Na2CO3+H2O.
(2)氢氧化钠溶液与盐酸分别显碱性、酸性,分别取少量的试剂与试管中,滴加无色酚酞溶液,变红色的是氢氧化钠溶液,不变色的是稀盐酸(合理即可).
故答案为:(1)①CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑;②CO2+2NaOH═Na2CO3+H2O;(2)分别取少量的试剂与试管中,滴加无色酚酞溶液,变红色的是氢氧化钠溶液,不变色的是稀盐酸(合理即可).
点评 物质的分离与鉴别是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.


科目:初中化学 来源: 题型:选择题
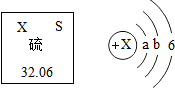 硫元素的信息如图所示,下列从图中获得的信息错误的是( )
硫元素的信息如图所示,下列从图中获得的信息错误的是( )| A. | 硫原子里,质子数=电子数=16 | |
| B. | 在硫原子的核外电子排布中a=2和b=8 | |
| C. | 一个硫原子的相对原子质量是32.06 g | |
| D. | 硫原子在化学反应中易获得2个电子形成S2- |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 打开浓盐酸的瓶盖,瓶口产生白烟 | |
| B. | 硫在空气中燃烧发出蓝紫色火焰,生成有刺激性气味的气体,并放出热量 | |
| C. | 取一段羊毛线,点燃,闻到有烧焦羽毛的气味 | |
| D. | 铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成黑色的四氧化三铁 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在氯化钠溶液中:Fe3+、NO3- | B. | 在稀盐酸中:Ag+、CO32- | ||
| C. | 在氢氧化钠溶液中:H+、Cu2+ | D. | 在硫酸铵溶液中:Ba2+、OH- |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | M的化学性质很稳定 | B. | M中有氨气 | ||
| C. | M由四种元素组成 | D. | M可能是碳酸氢钠 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
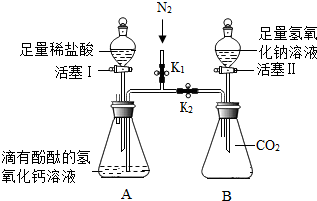 为了证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳能发生反应.如图所示进行实验(装置气密性良好,实验前弹簧夹K1、K2处于关闭状态)
为了证明氢氧化钙溶液与稀盐酸能发生反应,氢氧化钠溶液与二氧化碳能发生反应.如图所示进行实验(装置气密性良好,实验前弹簧夹K1、K2处于关闭状态)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com