
如图是用红磷燃烧法测定空气里氧气含量的装置图,有关此实验的结论与分析正确的是( )
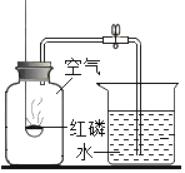
A. 此实验证明,氧气约占空气总质量的
B. 装置气密性不好,造成该实验测定结果偏大
C. 该实验中的红磷还可以用铁来代替
D. 反应后集气瓶内剩余的气体,既难溶于水,不可燃,也不支持燃烧
科目:初中化学 来源:河南省2019届九年级上学期期中考试化学试卷 题型:单选题
小明同学对化学反应A2+3B2═2C的理解错误的是( )
A. C的化学式为AB3
B. 若ag A2完全反应生成bg C,则同时消耗(b﹣a)g B2
C. 若mg A2和ng B2恰好完全反应,则生成(m+n)g C
D. 若A2和B2的相对分子质量分别为x和y,则C的相对分子质量为(x+y)
查看答案和解析>>
科目:初中化学 来源:浙江省温州市2019届九年级下学期中考一模化学试卷 题型:单选题
氘和氚是制造氢弹的原料.氘核和氚核在超高温的条件下会聚合成一个氦核,如图所示,下列说法正确的是( )
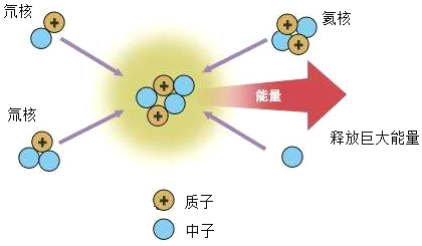
A. 氘和氚属于不同种元素 B. 氘原子、氚原子和氦原子的中子数均相同
C. 氘原子和氚原子的核电荷数分别为2,3 D. 氚原子的原子核有1个质子和2个中子构成
查看答案和解析>>
科目:初中化学 来源:重庆外国语学校2019届九年级上学期期中考试化学试卷 题型:综合题
某科学兴趣小组的同学设计了如下四个实验装置(天平略)来验证质量守恒定律。
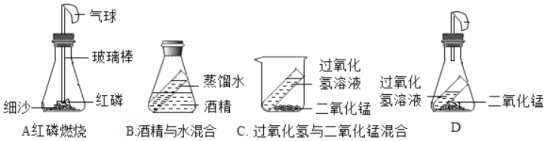
(1)上述的四个实验装置中_____装置能直接用于验证质量守恒定律;
(2)①装置A中发生反应的化学符号表达式:_____,实验过程中气球的变化是_____。
②点燃红磷的实验过程中,固体质量变化如图1所示:参加反应的氧气质量为_____g.
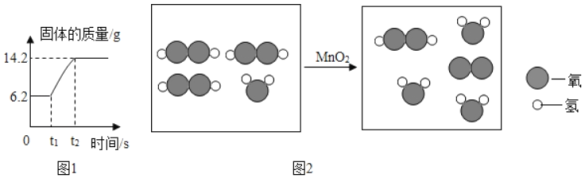
(3)C、D反应的微观示意图如图2所示,实际生成的物质分子数目之比为_____。
查看答案和解析>>
科目:初中化学 来源:重庆外国语学校2019届九年级上学期期中考试化学试卷 题型:单选题
在一定条件下,一个密闭容器内发生某反应,测得反应前后各物质的质量如下表所示。下列有关说法不正确的是( )
物质 | a | b | c | d |
反应前的质量/g | 30 | 20 | 10 | 15 |
反应后的质量/g | x | y | 0 | 10 |
A. x+y=65
B. x的取值范围,0≤x≤30
C. 当y≤20,该反应一定是化合反应
D. 参加反应的c与d的质量比为2:1
查看答案和解析>>
科目:初中化学 来源:重庆外国语学校2019届九年级上学期期中考试化学试卷 题型:单选题
下列推理不正确的是( )
①同种分子构成的物质,一定属于纯净物;
②只含一种元素的物质一定是单质;
③质子数相同的微粒一定是同种元素;
④含有氧元素的化合物一定是氧化物;
⑤最外层电子数相等的原子,化学性质一定相似;
⑥化学反应前后,原子的个数和种类一定不改变;
⑦同种物质中同种元素一定显相同价态。
A. ②③④⑤⑦ B. ②③④⑤⑥ C. ①②④⑥ D. ③④⑤⑦
查看答案和解析>>
科目:初中化学 来源:江苏省扬州市2019届九年级下学期第一次月考化学试卷 题型:科学探究题
碳酸钠广泛用于造纸、纺织、制革等工业,是一种重要的化工原料。我国侯德榜发明了将制碱与制氨结合起来的联合制碱法,为碳酸钠的工业化生产作出了巨大贡献。
(查阅资料)侯氏制碱法中主要反应:
Ⅰ.NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
Ⅱ.2NaHCO3=Na2CO3+H2O+CO2↑
(实验探究)小明以粗盐配制饱和食盐水,并采用如图1所示装置模拟制备碳酸氢钠,进而制得碳酸钠。

实验操作如下:
①关闭K1,打开K2通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②待三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。请回答下列问题:
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
剩余固体质量/g | 未记录 | 15.3 | 13.7 | 11.9 | 10.6 | 10.6 |
(1)粗盐中除了含有泥沙等不溶性杂质,还含有少量的MgCl2等。若要除去粗盐中的MgCl2,可加入过量的NaOH溶液,写出对应的化学方程式______,再过滤,然后向滤液中加入适量______,得到氯化钠溶液。
(2)饱和 NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为______。
(3)三颈烧瓶上连接的长颈漏斗的主要作用是______,有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是______;关闭K2停止通NH3后,还要继续通一段时间CO2,其目的是______。
(4)根据实验记录,计算t2时 NaHCO3固体的分解率(已分解的 NaHCO3质量与加热前原NaHCO3质量的比值),请写出计算过程_____。
(拓展延伸)小华设计如图2的实验装置测定某纯碱样品 (含少量杂质NaCl)中碳酸钠的质量分数:取一定量的样品与足量稀硫酸反应,通过排饱和碳酸氢钠溶液测定生成CO2的体积,计算样品中碳酸钠的质量分数。(已知常温常压下CO2的密度是1.977g/L)
(1)如果样品质量为5.3g,则实验中选用的量气管规格最合适的是______(填字母)。
A.500mL B.1000mL C.1500mL D.2000mL
(2)若实验中测得碳酸钠质量分数偏小,下列可能的原因是______。
a.装置漏气
b.读取数据时量气管的液面低于水准管的液面
c.反应结束后烧瓶中有CO2残留
d.读取数据时仰视读数
e.稀硫酸加入烧瓶占据体积
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com