
科目:初中化学 来源: 题型:实验探究题
 某同学对蜡烛的性质进行如下探究.
某同学对蜡烛的性质进行如下探究.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
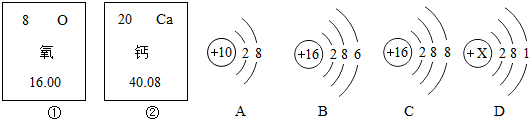
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲醛分子是由一个碳原子和一个水分子构成的 | |
| B. | 甲醛分子中C、H、O的原子个数之比为1:1:2 | |
| C. | 甲醛是由碳、氢、氧三种元素组成的 | |
| D. | 甲醛是由碳原子、氢分子和氧原子组成 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
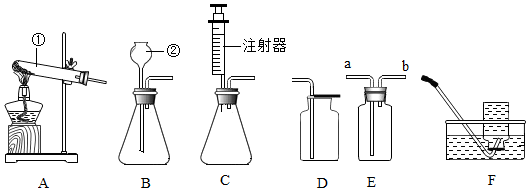
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢气+氧气$\stackrel{点燃}{→}$ 水 | B. | 碳酸钙$\stackrel{高温}{→}$氧化钙+二氧化碳 | ||
| C. | 乙醇+氧气$\stackrel{点燃}{→}$ 水+二氧化碳 | D. | 氢气+氯气$\stackrel{点燃}{→}$ 氯化氢 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
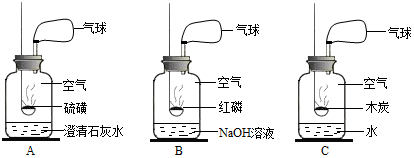
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com