
 某钙片的标签如图,且知钙片成分中只有碳酸钙中含有钙元素:
某钙片的标签如图,且知钙片成分中只有碳酸钙中含有钙元素:| 物质的质量 | |
| 反应前:烧杯+盐酸 | 22g |
| 10片钙片 | 8g |
| 反应后:烧杯+剩余物 | 26.7g |
分析 反应前总质量为22g+8g=30g,反应后变为26.7g,少了3.3g,过程中是碳酸钙和盐酸反应生成氯化钙、水喝二氧化碳,而二氧化碳是气体,生成后逸出,所以总质量减少量为生成的气体二氧化碳的质量,即二氧化碳的质量为3.3g,根据二氧化碳求算碳酸钙的质量,进而求算出钙元素的含量.
解答 解:根据质量守恒定律可知生成的二氧化碳的质量为22g+8g-26.7g=3.3g.
设参加反应的碳酸钙的质量为x,对应的钙元素的质量为y.根据反应CaCO3+2HCl=CaCl2+H2O+CO2↑和碳酸钙的化学式可得关系式如下
Ca∽∽∽CaCO3∽∽∽CO2↑
40 100 44
y x 3.3g
$\frac{40}{y}$=$\frac{100}{x}$=$\frac{44}{3.3g}$
x=7.5g
y=3g
由于过程中是取了10片钙片,所以每片的碳酸钙的质量为$\frac{7.5g}{10}$=0.75g,每片所含的钙元素的质量为$\frac{3g}{10}$=0.3g
答:①每片此钙片含碳酸钙的质量0.75g.
②每片此钙片的含钙量0.3g,厂家可以如下两种修改标签方式:a将“含钙量:每片含钙0.75g“改为”
含碳酸钙量:每片含碳酸钙0.75g;b将“含钙量:每片含钙0.75g“改为”含钙量:每片含钙0.3g;
本题也可以采用常规计算方式如下
解:根据质量守恒定律可知生成的二氧化碳的质量为22g+8g-26.7g=3.3g.
设参加反应的碳酸钙的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 3.3g
$\frac{100}{44}$=$\frac{x}{3.3g}$
x=7.5g
由于过程中是取了10片钙片,所以每片的碳酸钙的质量为$\frac{7.5g}{10}$=0.75g,每片所含的钙元素的质量为0.75g×$\frac{40}{40+12+16×3}$×100%=0.3g
答:①每片此钙片含碳酸钙的质量0.75g.
②每片此钙片的含钙量0.3g,厂家可以如下两种修改标签方式:a将“含钙量:每片含钙0.75g“改为”
含碳酸钙量:每片含碳酸钙0.75g;b将“含钙量:每片含钙0.75g“改为”含钙量:每片含钙0.3g.
点评 计算方法在平时可以多训练,注意方法的灵活性和一题多解的思考方式.


 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案科目:初中化学 来源: 题型:解答题
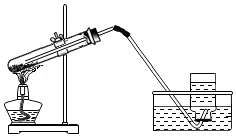 用右如图装置加热高锰酸钾制取氧气,指出装置中的三处错误:导气管插入试管太长、试管口向上倾斜、试管口没有棉花.
用右如图装置加热高锰酸钾制取氧气,指出装置中的三处错误:导气管插入试管太长、试管口向上倾斜、试管口没有棉花.查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 同种分子构成的物质一定是纯净物,所以纯净物一定由同种分子构成 | |
| B. | 同种元素质子数相同,所以质子数相同的粒子统称同种元素 | |
| C. | 物质和氧气发生的反应是氧化反应,所以发生氧化反应一定有氧气参加 | |
| D. | 化合物是由不同种元素组成的纯净物,所以由不同种元素组成的纯净物一定是化合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com