
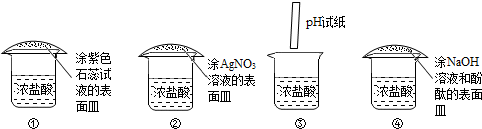
| A. | ①③ | B. | ② | C. | ④ | D. | ①②④ |
分析 证明“白雾”中含有氢离子即证明溶液呈酸性,所以能证明溶液呈酸性的反应就是证明了氢离子的存在,据此分析判断选项即可.
解答 解:浓盐酸瓶口的白雾是由浓盐酸挥发出的氯化氢气体与水蒸气结合而成的盐酸小液滴.
①石蕊试液遇酸性溶液变红色,所以涂有紫色石蕊的表面皿接触到“白雾”会变红,能证明“白雾”呈酸性,从而可说明溶液中含有氢离子;
②涂有硝酸银溶液的表面皿遇白雾会生成氯化银的白色沉淀,可说明白雾中含有氯离子;
③pH试纸可测量白雾的pH,从而可判断白雾(氯化氢与空气中的水蒸气结合成的盐酸小液滴)呈酸性,能证明氢离子的存在不能证明氯离子存在;
④氢氧化钠能使酚酞试液变红,所以涂有氢氧化钠和酚酞的表面皿是红色的,盐酸的小液滴能与氢氧化钠反应,使溶液碱性消失红色褪去,从而可证明“白雾”呈酸性,含有氢离子,不能证明含有氯离子;
观察选项可得答案.
故选B.
点评 此题是对酸性溶液性质的考查,掌握能证明溶液呈酸性(含有氢离子)的方法是解题的关键所在.


科目:初中化学 来源: 题型:解答题
| 分 类 | 分类标准 |
| 类别一:Fe、Cu 类别二:H2SO4、NaOH、NaCl、AgCl | 用元素种类为分类依据 |
| 类别一:Fe、Cu、AgCl 类别二:H2SO4、NaOH、NaCl | 用能否溶于水为分类依据 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
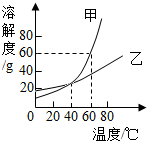 溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图回答下列问题:
溶解度曲线为我们定量描述物质的溶解性强弱提供了便利.请你根据如图回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氘氚 | B. | 浓缩铀 | C. | 优质煤 | D. | 高热值天然气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 海产品 | 非海产品 |
| 裙带菜(干)(15878 微克) | 稻米(2.3 微克) |
| 紫菜(干)(4323 微克) | 小麦面粉(2.9 微克) |
| 海带(鲜)(923 微克) | 猪肉(瘦)(1.7 微克) |
| 海虹(346 微克) | 牛肉(瘦)(10.4 微克) |
| 虾皮(264.5 微克) | 鲤鱼(4.7 微克) |
| 虾米(82.5 微克) | 小白菜(10 微克) |
| 金枪鱼(14 微克) | 番茄(2.5 微克) |
| 墨鱼(13.9 微克) | 芹菜(0.7 微克) |
| 带鱼(8.7 微克) | 茄子 (1.1 微克) |
| 小黄鱼(9.5 微克) | 橙子(0.9 微克) |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com