
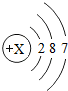 则该元素的原子序数为
则该元素的原子序数为

科目:初中化学 来源: 题型:
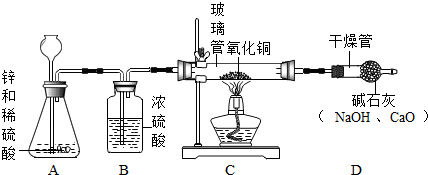
| A、实验说明:同种物质的溶液浓度大小不同时,化学性质可能不同 |
| B、实验中生成SO2的质量等于3.2g |
| C、实验中除了生成SO2,还会生成H2 |
| D、用此反应制ZnSO4虽有污染,但原料利用率高 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实验步骤 | 实验现象 | 实验结论 |
| 1、取样,加入足量的稀盐酸 | 有大量气泡产生,固体全部溶解, |
打火石中不含铁 |
| 2、另取样,加入足量的NaOH溶液 | 打火石中含有镁、铝 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
 2014年3月8日在马来西亚吉隆坡国际机场起飞后失联的MH370是波音777.飞机制造广泛采用新一代铝合金,同时在襟翼、扰流板、短舱和方向舵中采用碳复合材料.随科技发展,飞机不再金属专制,碳复合材料占比已超金属.
2014年3月8日在马来西亚吉隆坡国际机场起飞后失联的MH370是波音777.飞机制造广泛采用新一代铝合金,同时在襟翼、扰流板、短舱和方向舵中采用碳复合材料.随科技发展,飞机不再金属专制,碳复合材料占比已超金属.查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com