
分析 【对猜想的解释】(1)根据氧化钙和水反应氢氧化钙进行解答;
(2)根据氢氧化钙和碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠进行解答;
【实验结论】(3)根据碳酸钠溶液和氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠进行解答;
(4)根据酸碱中和的原理进行解答;
(5)根据氢氧化钠固体容易吸水潮解、易吸收空气中的CO2而变质进行解答.
解答 解:【对猜想的解释】(1)氧化钙和水反应氢氧化钙,化学方程式为:CaO+H2O═Ca(OH)2,所以料液中一定没有CaO;
(2)氢氧化钙和碳酸钠溶液反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH,所以料液中一定存在NaOH;
【实验结论】(3)碳酸钠溶液和氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,所以取适量料液放入试管中,滴加少量Na2CO3溶液,料液中出现白色沉淀,说明一定含有氢氧化钙,所以猜想①成立;
(4)蛋食用时加入一些食醋,可以去除涩感,原因是酸碱起中和反应,所以食醋可以去除松花皮蛋涩味的原因是:食醋中的酸(或醋酸)中和残留在皮蛋中的碱;
(5)氢氧化钠固体容易吸水潮解、易吸收空气中的CO2而变质,所以要密封保存,故选:AB.
故答案为:【对猜想的解释】(1)CaO+H2O═Ca(OH)2;
(2)Ca(OH)2+Na2CO3═CaCO3↓+2NaOH;
【实验结论】(3)①;
(4)食醋中的酸(或醋酸)中和残留在皮蛋中的碱;
(5)AB.
点评 本题是一道综合题,涉及的知识点较多,本题中掌握氢氧化钙与碳酸钠的反应是解题的关键.


 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 原子是一定比分子小的基本粒子 | |
| B. | 原子是一切变化中的最小粒子 | |
| C. | 原子是不能再分的粒子 | |
| D. | 原子的质量等于核内质子和中子的质量和 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 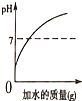 向一定质量的稀盐酸中不断加水,溶液的pH变化情况 | |
| B. | 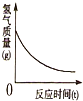 在密闭的硬质玻璃管中充满氢气,并盛有一定质量的氧化铜,加热反应时的氢气质 量变化情况 | |
| C. | 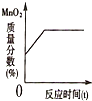 加热一定质量的氯酸钾和二氧化锰的混合物,二氧化锰在固体混合物中的质量分数 变化情况 | |
| D. | 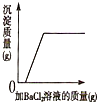 在一定质量的稀盐酸与硫酸钠的混合溶液中逐渐滴加氯化钡溶液,沉淀的变化情况 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
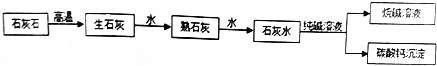
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色.
人类的生产生活离不开金属材料,随着科技水平的不断提高,金属及其合金在日常生活中扮演着越来越重要的角色.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
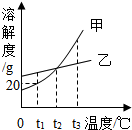
| A. | 甲物质的饱和溶液中含有少量乙,可采用降温结晶的方法分离提纯甲 | |
| B. | 将t2℃时的甲、乙两种物质的饱和溶液升温至t3℃(溶剂的量不变),两种溶液中溶质的质量分数相等 | |
| C. | t2℃时,要使接近饱和的乙溶液达到饱和状态,可采用蒸发溶剂的方法 | |
| D. | t1℃时,50g甲的饱和溶液中溶解了10g的甲 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,然后滴加足量的氯化钙溶液 | 产生白色沉淀,滤液变成无色(或滤液仍然是红色的) | 猜想正确 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com