
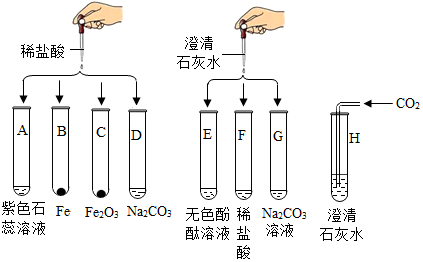
分析 (1)酸与金属反应生成盐和氢气,酸与碳酸盐反应生成盐、水、二氧化碳;根据反应后产物中有沉淀生成的实验考虑;
(2)在D试管中盛有无色酚酞试液,加入石灰水后,显碱性,溶液变红色,再向其中加入稀盐酸,当盐酸把氢氧化钙反应掉后,显酸性时,溶液变为无色;
(3)反应后有白色沉淀产生,滤液中必须含有碳酸根离子;
(4)实验后某试管中只得到无色溶液,向其中加入足量的Na2CO3溶液,无明显现象.说明试管内的物质与碳酸钠不反应,由此推断,该试管中是碳酸钠和盐酸反应生成了氯化钠、水和二氧化碳,原无色溶液中的溶质是NaCl或是氯化钠和碳酸钠的混合物.
解答 解:(1)碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,所以有沉淀生成的试管是GH;铁与盐酸反应生成氯化亚铁和氢气;碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,所以有气泡出现的试管是BD;
(2)在D试管中盛有无色酚酞试液,加入石灰水后,显碱性,溶液变红色,再向其中加入稀盐酸,当盐酸把氢氧化钙反应掉后,显酸性时,溶液变为无色;
(3)实验后某试管的底部有白色固体,即有白色沉淀生成,有沉淀生成的试管只有G和H;过滤后向滤液中滴加盐酸,一段时间后有气泡冒出,说明滤液中含有碳酸根离子,所以H不可能.该试管中最初发生反应的化学方程式:Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(4)实验后某试管中只得到无色溶液,向其中加入足量的Na2CO3溶液,无明显现象.说明试管内的物质与碳酸钠不反应,由此推断,该试管中是碳酸钠和盐酸反应生成了氯化钠、水和二氧化碳,原无色溶液中的溶质是NaCl或是氯化钠和碳酸钠的混合物.
故答案为:(1)GH;BD;
(2)稀盐酸;无色酚酞溶液;
(3)Na2CO3+Ca(OH)2=2NaOH+CaCO3↓;
(4)NaCl或是氯化钠和碳酸钠的混合物.
点评 本题容易出错的地方是第(3)小题,滤液中的溶质是往往忽略过量的碳酸钠,否则加入盐酸不能产生气泡,有的同学可能写上了碳酸钠,而忽略了反应产生的氢氧化钠..


 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验内容 | 实验方案设计 |
| A | 制取少量纯净的氢气 | 选用金属镁和浓盐酸反应,直接收集即可 |
| B | 除去粗盐中混有的Na2SO4 | 加入过量Ba(NO3)2溶液,过滤 |
| C | 检验实验室制取CO2的剩余废液中仍含有盐酸 | 加适量AgNO3溶液,产生白色沉淀即可证明 |
| D | 鉴别石灰水和氢氧化钠溶液 | 分别滴加Na2CO3溶液,变白色浑浊的是石灰水 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1个C原子和1个O2分子反应,生成2个CO2分子 | |
| B. | 32 g S与32 g O2完全反应,生成64 g SO2 | |
| C. | 镁条燃烧后固体质量增加,故质量守恒定律不是普遍规律 | |
| D. | 根据:蜡烛+氧气$\stackrel{点燃}{→}$二氧化碳+水,则蜡烛中一定含有C、H、O三种元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | P点表示甲、丙两种物质的饱和溶液中含溶质质量相等 | |
| B. | t1℃时,乙物质的饱和溶液,升温至t2℃时仍是饱和溶液 | |
| C. | t1℃时,甲物质的饱和溶液中溶质和溶剂的质量比为1:4 | |
| D. | 将甲、乙的饱和溶液分别从t2℃降至t1℃,甲析出晶体较多 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe→Fe2O3→FeCl2 | B. | CaCO3→CO2→CO | ||
| C. | CuO→Cu (OH)2→CuSO4 | D. | HNO3→NaNO3→NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
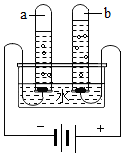 水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.请你回答:
水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.请你回答:查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com