

分析 (1)据常用仪器回答;
(2)据高锰酸钾制取氧气的反应原理书写方程式,装入药品前要先检查装置的气密性,防止装置漏气;制取较纯净的氧气,用排水法;
(3)发生装置依据反应物的状态及反应条件选择,不同的实验装置具有不同的特点;
(4)据氧气验满的方法解答.
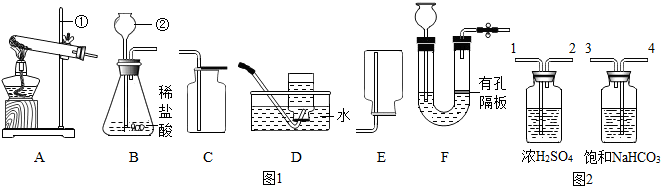
解答 解:(1)标号仪器分别是酒精灯、长颈漏斗;
(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,发生装置选择A;方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;制取较纯净的氧气,用排水法;
(3)实验室用二氧化锰和过氧化氢制取氧气,为固液常温反应,法装置选择B;分液漏斗可控制液体的滴加速度,从而达到控制反应速率的目的;
(4)若如图G装置用向上排空气法收集生成的氧气,气体应从c端通入,因氧气的密度比空气大;验满的方法是在d导管口放上带有火星的木条,如果木条复燃说明氧气已收满;
故答案为:(1)酒精灯、长颈漏斗;(2)A、F、2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+2O2↑;(3)B,分液漏斗或注射器;(4)c,在d导管口放上带有火星的木条,如果木条复燃说明氧气已收满.
点评 了解制取气体的反应原理、验满方法、常用仪器、收集方法所依据的知识,并能结合题意解答.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:选择题

| A. | 容器1的温度是900℃ | B. | 容器2中的固体Co比容器1中的纯净 | ||
| C. | 气体Y是CoCl2和H2 | D. | 杂质的沸点高于900℃ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 方案 | 实验操作 | 实验现象 | 结论 |
| 方案一 | 取少量滤液于试管中,在滤液中插入一根铜丝 | 铜丝表面无变化 | 猜想①成立 |
| 铜丝表面有银白色固体析出 | 猜想②成立 | ||
| 方案二 | 取少量滤液于试管中,滴加几 滴稀盐酸 | 滤液无明显变化 | 猜想①成立 |
| 生成白色沉淀 | 猜想②成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

 (注意标明二氧化碳、盐酸质量的相应数值).
(注意标明二氧化碳、盐酸质量的相应数值).查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 某固体中加入稀盐酸,产生无色气体,证明该固体中一定含有CO32- | |
| B. | 某溶液中加BaCl2溶液,生成不溶于稀硝酸的白色沉淀,则该溶液中一定含有SO42- | |
| C. | 某无色溶液滴入酚酞试液变红色,该溶液一定是碱溶液 | |
| D. | 验证烧碱溶液中是否含有Cl-,应先加硝酸除去OH-,再加AgNO3溶液,有白色沉淀出现,证明含有Cl- |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 将pH试纸投入待测液,对照标准比色卡读数 | |
| B. | 用干燥、洁净的玻璃棒蘸取少量待测液,沾在pH试纸上,根据试纸呈现颜色,对照标准比色卡读数 | |
| C. | 用玻璃棒蘸取待测液沾在用蒸馏水润湿的pH试纸上.对照标准比色卡读数 | |
| D. | 用玻璃棒蘸取待测液沾在pH试纸上晾干后再对照标准比色卡读数 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com