
将12.5克石灰石粉末(杂质不溶于水,也不参加反应)与100克稀盐酸恰好完全反应,反应中生成气体 4.4克;试求:
(1)石灰石的纯度。
(2)稀盐酸中溶质的质量分数。
(3)反应后所得溶液中溶质的质量分数。
(1)80%
(2)7.3%
(3)10.5%
解析试题分析:根据题意,石灰石样品与稀盐酸反应,生成氯化钙、水和二氧化碳,故反应的化学方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑,当石灰石粉末与稀盐酸恰好完全反应时,生成的二氧化碳质量4.4g,利用化学方程式中碳酸钙与二氧化碳的质量比,结合二氧化碳的质量,可求出样品中碳酸钙的质量,
进而算出石灰石的纯度,也可以利用HCl,CaCl2与二氧化碳的质量比,分别算出稀盐酸中溶质HCl的质量,进而算出稀盐酸中溶质的质量分数,反应后所得溶液中溶质CaCl2的质量,而反应后溶液的质量可以把反应前参加反应的物质质量减去生成的二氧化碳气体的质量,进而算出反应后所得溶液中溶质的质量分数
解,设石灰石样品中碳酸钙的质量为x,稀盐酸中HCl的质量为y,生成的CaCl2质量为z
CaCO3+ 2HCl=CaCl2+H2O+CO2↑
100 73 111 44
x y z 4.4g
(1)100:44=x:4.4g x=10g
∴石灰石的纯度=10g/12.5g×100% =80%
(2)73:44=y:4.4g y=7.3g
∴稀盐酸中溶质的质量分数=7.3g/100g×100%=7.3%
(3)111:44=z:4.4g z=11.1g
而反应后溶液质量=10g+100g-4.4g=105.6g
∴反应后所得溶液中溶质的质量分数=11.1g/105.6g×100%=10.5%


科目:初中化学 来源: 题型:计算题
进行如图所示的化学实验(装置气密性良好),通过二氧化碳中碳元素与氧元素的质量比来证明二氧化碳的组成,探究过程如下: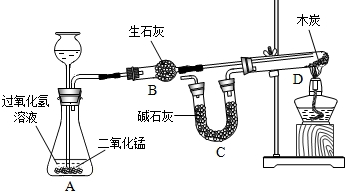
Ⅰ.称量有干燥块状木炭的试管D,质量为a g,装有碱石灰的C装置质量为b g,连接A、B、D装置;
Ⅱ.从长颈漏斗中加入3%的过氧化氢溶液,连接C装置,点燃酒精灯;
Ⅲ.待D中发生反应,熄灭酒精灯,冷却;
Ⅳ.称量试管D及剩余固体质量为cg,装置C的质量为dg;
已知:碱石灰用于吸收二氧化碳,木炭中的杂质不参加反应,B、C中所装药品能完全吸收相关物质.请回答下列问题:
①二氧化锰的作用是 ,装置B的作用是 ,B中发生反应的化学方程式为 ;
②为减少误差,步骤Ⅲ冷却过程中需要注意的问题是 ;
③除②中注意的问题外,该实验过程中还存在一定的误差,你认为产生误差的原因是 ;
④这个实验中如果生成的氧气的质量为16克,则需要参加反应的过氧化氢的物质的量为多少摩尔?(根据化学方程式计算,写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
将6.8 g含杂质的锌粒,加入到盛有50.0 g过量的稀硫酸的烧杯中(杂质不溶于水,也不与稀硫酸反应),充分反应后,称得烧杯内物质的总质量为56.6 g。试计算:
(1)生成氢气的质量。 (2)锌粒中所含锌的质量分数(精确到0.1%)。
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
某课外活动小组为测定当地石灰石中含碳酸钙的质量分数,取来了一些矿石,准确称取25g放于盛有200g稀盐酸(氯化氢的水溶液)的烧杯中(杂质不溶于水,也不与稀盐酸反应,也不分解),恰好完全反应。测得烧杯内物质的总质量与时间的关系如图所示(溶解的气体忽略不计)。
试计算:
(1)生成二氧化碳的质量是 _;
(2)所用稀盐酸的溶质质量分数是多少?
(3)石灰石中碳酸钙的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
实验室高温煅烧125g含CaCO380%的石灰石(杂质不分解也不与酸反应),一段时间后,停止实验,冷却后用剩余的固体处理废盐酸。问能否处理含70gHCl的废盐酸,请写出计算过程。
已知:CaCO3 CaO+ CO2↑
CaO+ CO2↑
CaO+2HCl=CaCl2+H2O
Ca(OH)2+2HCl=CaCl2+2H2O
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
现有铜与另一种金属的混合物粉末,另一种金属可能是镁、铁、锌中的一种,现欲测定其组成.
【查阅资料】(1)镁、铁、锌皆能与稀硫酸发生置换反应,且生成+2价的可溶性金属硫酸盐和氢气.
(2)相对原子质量:Mg﹣24、Fe﹣56、Zn﹣65
【实验步骤及数据】取该混合物粉末8.0g放入烧杯中,将140.0g 14.0%的稀硫酸分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如下:
| 次数 | 1 | 2 | 3 | 4 |
| 加入稀硫酸的质量/g | 35.O | 35.0 | 35.O | 35.O |
| 剩余固体的质量/g | 6.8 | 5.6 | 4.4 | 4.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
鸡蛋壳的主要成分是磷酸钙.为了测定某鸡蛋壳中碳酸钙的质量分数,小群同学进行了如下实验:将鸡蛋壳洗净、干燥并捣碎后,称取10g放在烧杯里,然后往烧杯中加入足量的稀盐酸90g,充分反应后,称得反应剩余物为97.14g.(假设其他物质不与盐酸反应)
(1)产生二氧化碳气体 g.
(2)计算该鸡蛋壳中碳酸钙的质量分数.
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
将12g的石灰石放入烧杯中,加入一定量的稀盐酸,待恰好完全反应后,测得产生4.4g气体(杂质不溶于水,也不参加反应)。
计算:该石灰石中钙元素的质量分数是多少?(结果保留整数)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com