
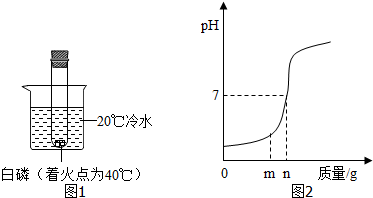
分析 (1)根据生石灰与水的反应分析回答;物质溶于烧杯中的冷水,能引起白磷燃烧,说明了物质在溶于水时能放出热量,据此分析.
(2)根据质量守恒定律可以书写化学方程式,根据化学方程式和图中情况可以进行相关方面的计算.
解答 解:(1)往烧杯中加入一定量生石灰会引起白磷燃烧,从燃烧条件分析,此时生石灰的作用是:生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点.将一定量的下列某物质溶于烧杯中的冷水,能引起白磷燃烧,说明了物质在溶于水时能放出热量,浓硫酸、氢氧化钠在溶于水时能放出热量,能使溶液的温度升高.
(2)氢氧化钙和盐酸反应能生成氯化钙和水,化学方程式为:Ca(OH)2+2HCl=CaCl2+2H20,
当加入熟石灰mg时,盐酸有剩余,溶液中的溶质是盐酸中的氯化氢和反应生成的氯化钙.故填:CaCl2和HCl.
由Ca(OH)2+2HCl=CaCl2+2H20; NaOH+HCl═NaCl+H2O 可知,氢氧化钙和盐酸反应的质量比是74:73.氢氧化钠和盐酸反应的质量比是80:73.加入ng氢氧化钙恰好完全反应,溶液显中性.加入ng氢氧化钠不能把盐酸反应完,即盐酸过量,溶液显酸性,PH<7.故填:<
故答案为:
(1)生石灰与水反应放出大量的热,水温升高,达到了白磷的着火点,浓硫酸、氢氧化钠;
(2)CaCl2和HCl;<.
点评 本题考查了燃烧的条件,明确物质溶于水或与水反应是否放热来分析.主要考查了化学方程式的书写及其根据图中信息进行相关方面计算的内容.


 手拉手全优练考卷系列答案
手拉手全优练考卷系列答案科目:初中化学 来源: 题型:推断题
 (1)某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和某种酸碱指示剂进行实验的过程见图. 如图所加试剂①②分别是氢氧化钠溶液、酚酞(指明具体物质的名称)
(1)某同学在探究“酸与碱能否发生反应”时,用稀NaOH溶液、稀盐酸和某种酸碱指示剂进行实验的过程见图. 如图所加试剂①②分别是氢氧化钠溶液、酚酞(指明具体物质的名称)查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 天然气用来作燃料 | B. | 二氧化碳用来作灭火 | ||
| C. | 干冰用作制冷剂 | D. | 氮气用作焊接金属的保护气 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 添加剂类别 | 主要作用 | 常见的添加剂 | 使用注意事项 |
| 防腐剂 | 抑菌防腐,延长保质期 | 亚硝酸钠、山梨酸钾等 | 绝不能超过安全标准 用量,否则有安全风险 |
| 酸化剂 | 改善食品的口味 | 柠梭酸,乳酸、苯甲酸等 | |
| 膨松剂 | 使食品蓬松 | 碳酸氢钠.碳酸氢铵等 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
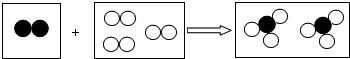 如图是某化学反应的微观模型,“○”“●”分别表示不同元素的原子,下列对图示模型的理解正确的是( )
如图是某化学反应的微观模型,“○”“●”分别表示不同元素的原子,下列对图示模型的理解正确的是( )| A. | 该反应属于分解反应 | |
| B. | 反应物和生成物中只有一种单质 | |
| C. | 参加反应的两种物质的分子个数比为2:3 | |
| D. | 共有两种元素参与反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 水是一种重要的自然资源.
水是一种重要的自然资源.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 实验目的 | 方案 |
| A | 鉴别硝酸钠溶液和硫酸钾溶液 | 取样,滴加Ba(NO3)2溶液,观察现象 |
| B | 除去粗盐中的难溶性杂质 | 将粗盐研碎、溶解、过滤、蒸发 |
| C | 确定某未知溶液中含有SO42- | 先滴加稀盐酸,无明显现象,再滴加BaCl2溶液,产生白色沉淀 |
| D | 除去CaO中的CaCO3 | 加入水溶解、过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com