
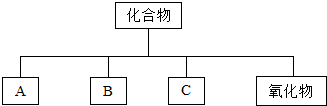
分析 (1)因化合物包括酸、碱、盐和氧化物,则根据Na、H、O、S元素组成的物质,结合图可知应分别为酸、碱、盐.
(2)因NaHSO4的溶液具有酸性,则可与碱或某些盐发生复分解反应.
解答 解:(1)结合常见化学概念之间的相互关系图,可知A、B、C为酸、碱、盐,则Na、H、O、S元素组成的酸为H2SO4;碱为NaOH;盐为Na2SO4或Na2SO3等;
故答案为:H2SO4;NaOH;Na2SO4或Na2SO3;
(2)NaHSO4的溶液具有酸性,能与NaOH及Na2SO3反应,
故答案为:
NaOH+NaHSO4=Na2SO4+H2O;2NaHSO4+Na2SO3=2Na2SO4+H2O+SO2↑.
点评 学生应熟悉化合物的分类,根据化合物中的元素组成和性质来认识酸、碱、盐,并能根据复分解反应发生的条件来书写相关的化学反应方程式.


科目:初中化学 来源: 题型:解答题
| OH- | CO32- | SO42- | NO3- | |
| Ba2+ | 溶 | 不 | 不 | 溶 |
| Cu2+ | 不 | 不 | 溶 | 溶 |
| Li+ | 溶 | 微溶 | 溶 | 溶 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 16:9 | B. | 23:9 | C. | 32:9 | D. | 46:9 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | b-a=d-c | B. | a-n=c+m | C. | a+n=c-m | D. | b-n=d+m |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 操作 | 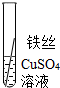 | 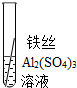 | 根据现象得出金属活动性顺序 |
| 现象 | 无明显现象 | 无明显现象 | Al>Fe>Cu |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
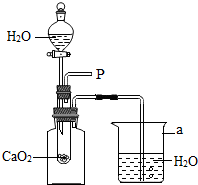 小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.
小强在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小强共同探究.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com