
分析 金属具有良好的导电性、导热性和延展性;
金属越活泼,人类开发利用的就越晚;
通常情况下,铝能和空气中的氧气反应生成氧化铝保护膜;
加热条件下,氧化铜和氢气反应生成铜和水,根据反应的化学方程式和提供的数据可以进行相关方面的计算.
解答 解:(1)物质的性质决定物质的用途.由于铜具有良好的导电性,所以铜常用于制作导线.
故填:导电.
(2)常见的三种金属被发现和使用的先后顺序依次为:铜、铁、铝.金属大规模被使用的先后顺序跟金属的活动性关系最大.
故填:③.
(3)铝在空气中表现良好的抗腐蚀性能,是因为铝能和空气中的氧气反应生成氧化铝,反应的化学方程式为:4Al+3O2═2Al2O3.
故填:4Al+3O2═2Al2O3.
(4)有铜和氧化铜的混合物10g,通入氢气加热至完全反应,冷却后称量剩余固体的质量为8.4g.
①氧化铜与氢气反应的化学方程式为:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
故填:CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
②设该混合物中氧化铜的质量为x,
CuO+H2$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,固体质量减小
80 64 80-64=16
x 10g-8.4g=1.6g
$\frac{80}{x}$=$\frac{16}{1.6g}$,
x=8g,
故填:8.
点评 本题主要考查物质的性质,只有掌握了各种物质的性质,才能够判断物质之间相互转化时的反应物和生成物,从而可以进行各方面的判断.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
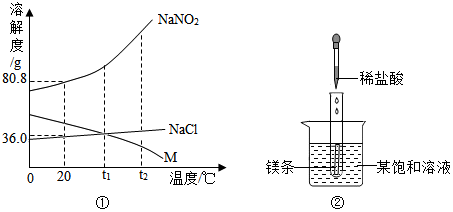
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水是一种最常见的溶剂 | B. | 水是由氢元素和氧元素组成 | ||
| C. | 水分子保持水的化学性质 | D. | 水分子由氢分子和氧分子构成 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 实验后剩余的药品应该放回原瓶,避免浪费 | |
| B. | 不小心碰倒酒精灯,洒出的酒精在桌子上燃烧起来,应立即用水扑灭 | |
| C. | 用pH试纸测定溶液酸碱度时,先将pH试纸用水润湿,然后再进行测定 | |
| D. | 洗过的玻璃仪器内壁附着的水既不聚成水滴,也不成股流下时,表明已经洗干净 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
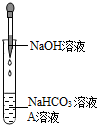 同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.
同学们发现NaOH溶液与NaHCO3溶液混合后无明显现象,产生疑问:两种物质是否发生了化学反应?在老师的帮助下,他们通过以下探究过程证明NaHCO3溶液与NaOH溶液发生了反应.| NaHCO3溶液 | NaOH溶液 | Na2CO3溶液 | |
| 加入稀盐酸 | 现象Ⅰ | 无明显变化 | 产生气泡 |
| 加入澄清石灰水 | 溶液变浑浊 | 无明显变化 | 现象Ⅱ |
| 加入CaCl2溶液 | 无明显变化 | 溶液变浑浊 | 溶液变浑浊 |
| 加热溶液至沸腾,将 气体通入澄清石灰水 | 澄清石灰水 变浑浊 | 澄清石灰水 无明显变化 | 澄清石灰水 无明显变化 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
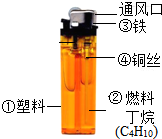 打火机给人们的生活带来了方便,如图是普通打火机的示意图.据图回答:
打火机给人们的生活带来了方便,如图是普通打火机的示意图.据图回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
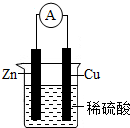 资源、能源、环境与人类的生活和社会发展密切相关.
资源、能源、环境与人类的生活和社会发展密切相关.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com