
| A. | 溶液选种 | B. | 作融雪剂 | C. | 作调味品 | D. | 制碳酸钠 |
分析 物质的化学性质是指在化学变化中表现出来的性质,物质的物理性质是指不需要通过化学变化表现出来的性质,据此进行分析判断.
解答 解:A、氯化钠溶液选种,不需要发生化学变化就能表现出来,是利用了其物理性质,故选项错误.
B、氯化钠作融雪剂,是利用了氯化钠能降低雪凝固点的性质,不需要发生化学变化就能表现出来,是利用了其物理性质,故选项错误.
C、氯化钠作调味品,是利用了氯化钠有咸味的性质,不需要发生化学变化就能表现出来,是利用了其物理性质,故选项错误.
D、氯化钠制碳酸钠,需要通过化学变化才表现出来,是利用了其化学性质,故选项正确.
故选D.
点评 本题难度不大,区分物质的用途是利用了物理性质还是化学性质,关键就是看利用的性质是否需要通过化学变化体现出来.


科目:初中化学 来源: 题型:选择题
| A. | 有机物:甲烷、乙醇、葡萄糖 | |
| B. | 复合肥料:尿素、硝酸钾、磷酸氢二铵 | |
| C. | 混合物:煤、石油、冰水共存物 | |
| D. | 合成材料:合金、合成橡胶、合成纤维 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 其相对原子质量为165 | |
| B. | 其中钠、铁、氧三种元素质量比是2:1:4 | |
| C. | 其一个分子中含有7个原子 | |
| D. | 其中铁元素的质量分数为27.71% |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 棉线和羊毛线(点燃,闻气味) | B. | 过磷酸钙和氯化铵(观察颜色) | ||
| C. | 氧化铜粉末和铁粉(稀硫酸) | D. | 氢氧化钠溶液和石灰水(稀盐酸) |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
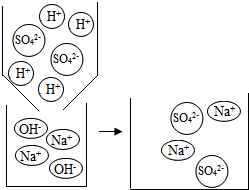
| 实验方案 | ①测溶液pH | ②滴加Na2CO3溶液 | ③滴加BaCl2溶液 |
| 实验现象 | 试纸变色,与标准比色卡比照,得pH<7 | 有气泡产生 | 产生白色沉淀 |
| 实验结论 | 溶液中有H2SO4 | 溶液中有H2SO4 | 溶液中有H2SO4 |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
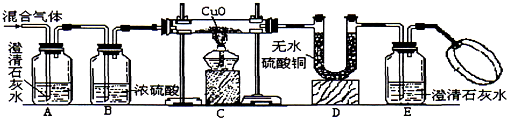
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com