
【题目】材料是人类赖以生存和发展的重要物质,目前使用量最多的金属材料仍然是钢铁。
(一)实验室用赤铁矿模拟工业炼铁的化学方程式为_____,炼得的铁是_____(填“单质铁”或“合金”),该反应_____(填“是”或“不是”)置换反应。
(二)FeCO3是菱铁矿的主要成分,具有还原性,在空气中灼烧生成铁的氧化物和CO2气体。要探究碳酸亚铁和氧气充分反应后的固体成分,请你参与小华同学的探究:
(查阅资料)
① FeO是一种黑色粉末,它不稳定,在空气中加热,就迅速被氧化成四氧化三铁,四氧化三铁能与盐酸反应生成氯化亚铁、氯化铁和水。
②FeCl2能使高锰酸钾溶液褪色,而FeCl3不能;FeCl3溶液中滴加KSCN溶液,溶液变红色,FeCl2溶液中滴加KSCN溶液,溶液不出现红色。
(猜想与假设)
猜想1:固体成分是氧化铁;
猜想2:固体成分是四氧化三铁;
猜想3:_____。
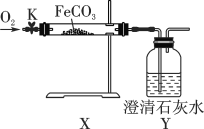
(活动与探究)连接仪器、装好药品如图所示(加热和固定装置已省略),打开止水夹K,通入氧气,加热玻璃管X。当Y瓶中产生的沉淀不再增加时,停止加热,继续通入氧气至玻璃管冷却。取玻璃管里的少量固体于试管中,滴加盐酸,微热,固体完全溶解。将所得溶液分成甲、乙两份进行实验。
实验编号 | 实验步骤 | 实验现象 |
a | 向甲溶液中滴加KSCN溶液 | 溶液变红色 |
b | 向乙溶液中滴加酸性高锰酸钾溶液 | 高锰酸钾溶液的紫红色不消失 |
(结论与反思)
(1)由上述实验现象可知,FeCO3在氧气中高温灼烧得到的固体产物是_____,因此,猜想_____(填“1”“2”或“3”)是正确的。
(2)FeCO3在氧气中高温灼烧的化学方程式为_____。
(3)上述实验_____(填“a”或“b”)是多余的,因为_____。
(总结与提升)
(1)若实验结束时观察到Y瓶中仍然是澄清的,可能的原因是澄清石灰水的量不足,导致生成的碳酸钙转变成了可溶于水的碳酸氢钙。碳酸氢钙的化学式为_____。
(2)CO2使澄清石灰水变浑浊的化学方程式为_____。
(3)华雪同学经过反思,觉得该实验设计还存在问题,因为如果在实验b中观察到_____,就不能确定哪个猜想是正确的。所以小华同学又对该实验进行了定量探究:取11.6 g纯净的碳酸亚铁固体,在空气中高温灼烧至恒重,称得固体质量净减3.6 g。通过计算即可确定:FeCO3和氧气充分反应后的固体成分是_____。
【答案】3CO+Fe2O3![]() 2Fe+3CO2 合金 不是 固体成分是氧化铁和四氧化三铁 氧化铁 1 4FeCO3+O2
2Fe+3CO2 合金 不是 固体成分是氧化铁和四氧化三铁 氧化铁 1 4FeCO3+O2![]() 2Fe2O3+4CO2 a 无论是哪种猜想中的固体,溶于盐酸后溶液中都存在Fe3+,加入KSCN溶液后都会变红色,因此实验a不能判断固体的成分 Ca(HCO3)2 CO2+Ca(OH)2═CaCO3↓+H2O 高锰酸钾溶液褪色 氧化铁
2Fe2O3+4CO2 a 无论是哪种猜想中的固体,溶于盐酸后溶液中都存在Fe3+,加入KSCN溶液后都会变红色,因此实验a不能判断固体的成分 Ca(HCO3)2 CO2+Ca(OH)2═CaCO3↓+H2O 高锰酸钾溶液褪色 氧化铁
【解析】
解:(一)氧化铁和一氧化碳在高温的条件下生成铁和二氧化碳,化学方程式为:3CO+Fe2O3![]() 2Fe+3CO2;炼得的铁是合金,置换反应是单质与化合物反应生成单质与化合物的反应,所以该反应不是置换反应;
2Fe+3CO2;炼得的铁是合金,置换反应是单质与化合物反应生成单质与化合物的反应,所以该反应不是置换反应;
(二)[猜想与假设]由假设①②,也可能是两者的混合物,则猜想3是固体成分是氧化铁和四氧化三铁;
[结论与反思](1)由FeCl3溶液中滴加KSCN溶液,溶液变红色,FeCl2溶液中滴加KSCN溶液,溶液不出现红色,则向甲溶液中滴加KSCN溶液,溶液变红色,说明溶液中含有FeCl3;FeCl2能使高锰酸钾溶液褪色,而FeCl3不能,向乙溶液中滴加高锰酸钾溶液,高锰酸钾溶液的紫红色不消失,说明溶液中不含FeCl2;
氯化铁是氧化铁与稀盐酸反应生成的,所以FeCO3在氧气中高温灼烧得到的固体产物是氧化铁,因此猜想1是正确的;
(2)FeCO3在氧气中高温灼烧生成氧化铁和二氧化碳气体,化学方程式为:4FeCO3+O2![]() 2Fe2O3+4CO2;
2Fe2O3+4CO2;
(3)上述实验中a是多余的,无论是哪种猜想中的固体,溶于盐酸后溶液中都存在Fe3+,加入KSCN溶液后都会变红色,因此实验a不能判断固体的成分;
[总结与提升](1)碳酸氢钙中钙元素显+2价,碳酸氢根显-1价,其化学式为:Ca(HCO3)2;
(2)CO2使澄清石灰水变浑浊,是因为与氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为:CO2+Ca(OH)2═CaCO3↓+H2O;
(3)FeCl2能使高锰酸钾溶液褪色,而FeCl3不能,如果在实验b中观察到高锰酸钾溶液褪色,说明含有氯化亚铁溶液,不能确定是否含有氯化铁,就不能确定哪个猜想是正确的;华雪同学又对该实验进行了定量探究:取11.6g纯净的碳酸亚铁固体,在空气中高温灼烧至恒重,称得固体质量净减3.6g;假设生成的固体为氧化铁,设固体质量净减质量为x,
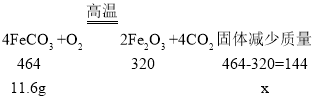
![]()
x=3.6g;假设成立,FeCO3和氧气充分反应后的固体成分是氧化铁。


科目:初中化学 来源: 题型:
【题目】地球深处的水处于超临界状态,称为超临界水。下图为某压强下CaCl2 和NaCl 在超临界水中的溶解度曲线,该压强下,下列说法正确是( )
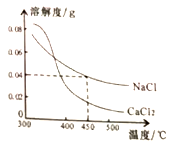
A.在超临界水中,NaCl的溶解度大于CaCl2的溶解度
B.在超临界水中,2种物质的溶解度都随温升高而增大
C.450℃时,NaCl在超临界水的溶解度为 0.04g
D.450℃时,可得到 0.04%的CaCl2的超临界水溶液
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如下图所示,下列关于该过程的说法正确的是()
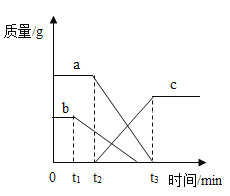
A.c代表氧气
B.t2时刻,O2开始产生
C.t1时刻,KMnO4开始分解
D.KMnO4质量在反应前后不变
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下表是元素周期表中第2、3周期的元素,请回答有关问题。
2 | 3 锂 6.941 | 4 铍 9.012 | 5 硼 10.81 | 6 碳 12.01 | 7 氮 14.01 | 8 氧 16.00 | 9 氟 19.00 | 10 氖 20.18 |
3 | 11 钠 22.99 | 12 镁 24.31 | 13 铝 26.98 | 14 硅 28.09 | 15 磷 30.97 | 16 硫 32.06 | 17 氯 35.45 | 18 氩 39.95 |
(1)铝元素的相对原子质量为________________;
(2)下列各组具有相似化学性质的元素是_______________(填字母序号);
A![]() B
B![]() C
C![]() D
D![]()
(3)第8号元素与第13号元素的原子形成化合物的化学式为_______________;
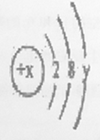
(4)某粒子的结构如图,当![]() 时,该粒子的符号为_______________;
时,该粒子的符号为_______________;
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】现有H、C、O、S、N、Cu、Ca七种元素,请从中选择适当的元素组成符合要求的物质,并按要求填空。
(1)A为碳不充分燃烧的生成物,写出A物质的化学式:_____。
(2)B为最简单的有机物,写出B物质在空气中燃烧的化学方程式:_____。
(3)C为实验室常用燃料,写出C物质的化学式:_____,C物质还可以通过淀粉类粮食发酵制得,淀粉的化学式_____。
(4)D为澄清石灰水的溶质,标出D物质中显正价元素的化合价:_____。
(5)E的水溶液为蓝色,且工业上常用E和D配制波尔多液,写出配制波尔多液的化学反应方程式_____;E中阴离子的离子符号为_____。
(6)F为一种常见的化肥,若与D混用,会产生_____(填化学式)降低肥效。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知A、C是无色液体,B、F、G是无色气体,其中大量排放F会引起温室效应,D是黑色固体, E在纯净的B中燃烧发出明亮的蓝紫色火焰。

(1)请写出下列物质的化学式:D________,E________,G________,H________。
(2)请写出下列变化的化学方程式:
①B→F,___________________。
②A→C,___________________。
③B→G,___________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钙是人体必需的常量元素,每日必须摄入足够量的钙。目前市场上的补钙药剂很多,如图是某种品牌的补钙药品的部分说明书。请回答下列问题:

(1)CaCO3中钙元素的质量分数为________。
(2)若每片钙片的质量为1 g,则钙片中钙元素的质量分数为_______。
(3)如果按用量服用,通过服用此钙片,每天摄入钙元素的质量是多少?______
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】我国化学家傅鹰教授有一句名言“科学只给我们知识,而历史却给我们智慧”在化学学习中,了解知识的发展历程,可以促进我们正确理解科学本质。
(1)我国西汉时期就有“曾青得铁则化为铜”的记载,期中蕴涵的湿法冶铜原理为 (用化学方程式表示)。
(2)火药起源于唐朝。为使烟火产生耀眼的白光,可在其火药中加入 (填一种金属名称)。
(3)十八世纪,化学家们研究发现某些金属与酸反应能生成一种气体,该气体被喻为“会制造水的物质”,对上述反应原理的认识加快了推翻燃素学说的进程。该气体在空气中燃烧制造水的化学方程式是 。
(4)现代以来,人们对金属的认识不断深入,助推多种新材料的研制与使用。2017年5月5日我国首架试飞成功的大型客机C919使用了多种新材料,其中有锂铝合金,在飞机制造中使用该材料说明其具有的有点有 (填序号)。
①硬度大 ②密度小 ③易导电 ④耐腐蚀
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】生产生活中离不开水,我们可以从不同角度认识水
(1)下列有关水净化的说法不正确的是___________(填序号)。
a 加热煮沸可降低水的硬度
b 过虑可以使硬水转化为软水
c 净水时活性炭起吸附作用
d 明矾可以将天然水消毒
(2)区分软硬水是把___________分别滴加到盛有等量的软水,硬水的试管中振荡,观察了试管中产生泡沫的情况。
(3)如图所示,电解水的实验中试管a、b中产生气体的体积比约为______,该实验验证明水是由_____组成的。
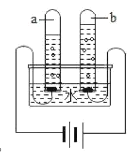
(4)每个水分子是由两_____________构成的。
(5)水能与许多物质发生化学反应,将二氧化氮和氧气混合气体通入水中生成硝酸,该反应的化学方程式为__________,该反应的基本类型属于______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com