
 据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染.同学们对废旧手机中的金属回收产生兴趣.
据统计,我国每年报废的手机超过1亿部,若不进行有效回收利用,会造成巨大的浪费和污染.同学们对废旧手机中的金属回收产生兴趣.| 种类 | Fe | Cu | Al | Ni | Au | Ag | Pd(钯) |
| 市场价格($/t) | 365 | 7175.5 | 1710.5 | 14235 | 4.7×107 | 7.6×105 | 2.7×107 |
| 矿石中含量 | 72.4 | 0.87 | 29.1 | 1.02 | 4 | 120 | 0.4 |
| 手机电路板中含量 | 5 | 13 | 1 | 0.1 | 350 | 1380 | 210 |
| 序号 | 实验步骤 | 实验现象 |
| I | 取一废旧手机电路板,用电吹风机靠近电路焊接点的焊锡吹热风,一段时间后,用镊子将金属电路从塑料板中拽出 | 焊锡熔化 |
| II | 将金属电路放入烧杯中,加入足量稀盐酸浸泡 | 溶液变成绿色,有无色气泡产生 |
| III | 取II中未溶解的金属电路,用蒸馏水洗净后,放入如右图所示装置中,进行实验.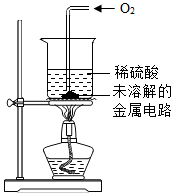 | 溶液逐渐变成蓝色,仍有微量金属固体未溶解 |
| IV | 过滤III中烧杯中的物质,洗涤滤纸上的物质 | 滤纸上仍有微量金属固体 |
| V | 向IV中得到的滤液中加入铁片 | 得到红色固体 |
分析 【实验方案】根据表格中的信息进行分析判断即可.
【问题讨论】(1)由步骤I中的现象焊锡熔化分析焊锡的物理性质.
(2)根据铁、镍和盐酸反应的原理以及氯化亚铁溶液、NiCl2溶液都为绿色进行分析.
(3)根据Fe、Al、Ni排在氢的前面进行分析.
(4)因为现象是得到红色固体,因此步骤V的操作是向IV中得到的滤液中加入铁片.
【反思交流】为了确认步骤IV中滤纸上的金属成分,还应知道Au、Ag、Pd在加热条件下,能否与氧气、稀硫酸发生反应.
解答 解:【实验方案】②Au、Ag、Cu、Pd在收集电路板中的含量高于其在矿石中的含量.
【问题讨论】(1)由步骤I中的现象焊锡熔化,可推知的焊锡的物理性质是熔点低.
(2)将金属电路放入烧杯中,加入足量稀盐酸浸泡,铁与盐酸反应生成氯化亚铁和氢气,氯化亚铁溶液是绿色的,镍与盐酸反应生成NiCl2溶液也为绿色,步骤II对应的实验现象是溶液变成绿色,有无色气泡产生.
(3)将金属电路放入烧杯中,加入足量稀盐酸浸泡,因为Fe、Al、Ni排在氢的前面,因此步骤II所得溶液中,一定含有的金属元素是Fe、Al、Ni.
(4)因为现象是得到红色固体,因此步骤V的操作是向IV中得到的滤液中加入铁片,铁置换出硫酸铜中的铜.
【反思交流】为了确认步骤IV中滤纸上的金属成分,还应知道Au、Ag、Pd在加热条件下,能否与氧气、稀硫酸发生反应.
故填:【实验方案】②Au、Ag、Cu、Pd在收集电路板中的含量高于其在矿石中的含量;溶液变成绿色,有无色气泡产生;向IV中得到的滤液中加入铁片.
【问题讨论】(1)熔点较低;(2)溶液变成绿色,有无色气泡产生; (3)Fe、Al、Ni;(4)向IV中得到的滤液中加入铁片;【反思交流】Au、Ag、Pd在加热条件下,能否与氧气、稀硫酸发生反应.
点评 此题难度较大,掌握金属的活动性以及根据题中信息分析问题的能力等即可顺利解答.


科目:初中化学 来源: 题型:选择题
| A. | 将煤进行液化、汽化 | B. | 开发风能、水能、氢能 | ||
| C. | 将热电厂的烟囱加高 | D. | 加强对汽车尾气排放的监控 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| OH- | NO3- | Cl- | SO42- | CO32- | |
| H+ | 溶、挥 | 溶、挥 | 溶 | 溶、挥 | |
| Na+ | 溶 | 溶 | 溶 | 溶 | 溶 |
| Ba2+ | 溶 | 溶 | 溶 | 不 | 不 |
| Ca2+ | 微 | 溶 | 溶 | 微 | 不 |
| Cu2+ | 不 | 溶 | 溶 | 溶 | 不 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 归类是我们经常用到的一种学习方法.若用下图所示的形式对所学知识进行归类,则表中的选项与图相符的是( )
归类是我们经常用到的一种学习方法.若用下图所示的形式对所学知识进行归类,则表中的选项与图相符的是( ) | 选项 | 甲 | X | Y | Z |
| A | 常见的碱 | 烧碱 | 纯碱 | 熟石灰 |
| B | 常见的有机物 | 甲烷 | 尿素 | 醋酸 |
| C | 常见的合金 | 钢铁 | 生铁 | 氧化铁 |
| D | 常见的酸 | 硫酸铜 | 盐酸 | 磷酸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 请回答:胃酸的主要成分是盐酸,胃酸过多会引起胃痛.右图是一种治疗胃病药物的标签.
请回答:胃酸的主要成分是盐酸,胃酸过多会引起胃痛.右图是一种治疗胃病药物的标签.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com