
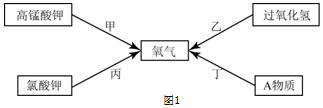
分析 (1)根据工业上分离液态空气制取氧气是利用液态氧和液态氮的沸点不同而分离出氧气进行分析;
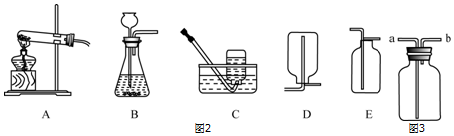
(2)①根据实验室制取氧气时的组装仪器的顺序进行分析;根据高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气进行分析;
②根据氧气的密度比空气大,不易溶于水进行分析;
③根据反应物状态和反应条件选择发生装置,根据气体密度和溶解性选择收集装置;
④根据分液漏斗可以控制液体的滴加速度进行分析;
(3)根据氢气密度比空气小进行分析;根据氧气不易溶于水,氧气密度比水小进行分析.
解答 解:(1)工业上分离液态空气制取氧气,根据液态氧和液态氮的沸点不同而分离出氧气,空气属于混合物;
(2)①在组装A装置时,应先放好酒精灯,然后根据酒精灯的高度来安装试管;高锰酸钾在加热的条件下生成锰酸钾、二氧化锰和氧气,反应的符号表达式为::2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
②氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;用排水法收集氧气时,收集满的现象是:当大气泡从集气瓶口向外冒出时,证明满了;
③实验室常用氯化铵固体与碱石灰固体共热来制取氨气.是加热固体制取气体,应选择的发生装置是A;由于氨气密度比空气小,氨气极易溶于水,只能用向下排空气法收集,收集装置可选用D;
④分液漏斗可以控制液体的滴加速度,所以要在实验中得到平稳的氧气流,可将上述装置中的长颈漏斗换为分液漏斗;
(3)若用排空气法收集比空气轻的气体时,应用向下排空法收集,采用短进长出的方法,因为氢气密度比空气小,气体应从装置的b端通入;氧气不易溶于水,氧气密度比水小,所以用如图3所示装置收集氧气,气体应从b端管口通入.
故答案为:(1)混合物;(2)①前;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;②氧气的密度比空气大;当大气泡从集气瓶口向外冒出时,证明满了;③A;D;④分液漏斗;(3)b;b.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.


科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
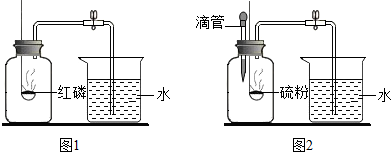 “空气中氧气含量的测定”有多种方法.甲生设计了如图1如示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:
“空气中氧气含量的测定”有多种方法.甲生设计了如图1如示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com