
| 物质 | 乙烷 | 丙烷 | 丁烷 | 戊烷 | 己烷 |
| 沸点/℃ | -88.6 | -42.2 | -0.5 | 36.1 | 69.2 |
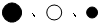 ”表示氧原子、碳原子、氢原子,则一个丙醇分子则可用下列哪种符号表示?Ⅷ.
”表示氧原子、碳原子、氢原子,则一个丙醇分子则可用下列哪种符号表示?Ⅷ.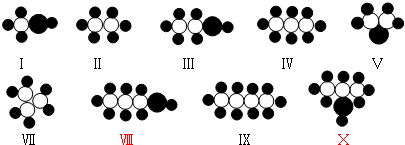
分析 (1)观察图表了解各种物质的沸点,然后必须明白常温是指20℃左右,看哪种物质在常温下是不能达到沸点即是剩余的物质.
(2)根据物质具有可燃性来分析;
(3)根据质量守恒定律结合数据进行分析.
解答 解:(1)观察图表可知,戊烷和己烷在常温常压下不能达到沸点,所以钢瓶中剩余的物质最有可能是戊烷和己烷.
故选D.
(2)这些液体具有可燃性,随意倾倒可能发生火灾或爆炸,故填:不能随意倾倒,以防发生火灾或爆炸;
(3)丙醇中碳元素的质量为:13.2g×$\frac{12}{44}×100%$=3.6g;氢元素的质量为:7.2g×$\frac{1×2}{18}×100%$=0.8g;
生成物中氧元素的质量为:13.2g+7.2g-3.6g-0.8g=16g
所以丙醇中含有氧元素,其质量为:16g-14.4g=1.6g
丙醇中,碳、氢、氧三种元素的质量比为:3.6g:0.8g:1.6g=9:2:4;
丙醇分子中,碳、氢、氧的原子个数比为:$\frac{3.6g}{12}$:$\frac{0.8g}{1}$:$\frac{1.6g}{16}$=3:8:1,化学式为CH3CH2CH2OH.
故填:①碳、氢、氧;②碳、氢、氧三种元素的质量比为9:2:4;③Ⅷ.
点评 做好此题首先看好图表,观察各种物质的沸点,然后确定可能剩余的物质.


 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案科目:初中化学 来源: 题型:选择题
| A. | 大理石 | B. | 钢铁 | C. | 陶瓷 | D. | 铝合金 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间/S | 0 | 30 | 60 | 90 | 120 | 150 | 180 |
| 增加的质量/g | 0 | 30 | 50 | 60 | 66 | 66 | 66 |

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
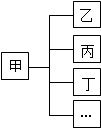 分类法是一种行之有效、简单易行的科学方法,人们在认识食物时可以采取多种分类方法.小军用如图所示形式对所学知识进行归纳,其中甲包括了乙、丙、丁…下列关系中,有错误的一组是( )
分类法是一种行之有效、简单易行的科学方法,人们在认识食物时可以采取多种分类方法.小军用如图所示形式对所学知识进行归纳,其中甲包括了乙、丙、丁…下列关系中,有错误的一组是( ) | 选项 | 甲 | 乙、丙 |
| A | 常见的干燥剂 | 浓硫酸、碱石灰、生石灰 |
| B | 常见的合金 | 不锈钢、焊锡、生铁 |
| C | 常见的碱 | 烧碱、纯碱、熟石灰 |
| D | 常见的营养物质 | 蛋白质、维生素、无机盐 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在科学学习中使用模型可以反映客观现象,简单明了地表示事物.如图:
在科学学习中使用模型可以反映客观现象,简单明了地表示事物.如图:查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 时间/min | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| 阴极上产生的气体体积/cm3 | 6 | 12 | 20 | 29 | 39 | 49 | 59 | 69 | 79 | 89 |
| 阳极上产生的气体体积/cm3 | 2 | 4 | 7 | 11 | 16 | 21 | 26 | 31 | 36 | 41 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com