

分析 (1)根据乙醇汽油的性质和特点判断.
(2)根据信息“汽车尾气中含有CO、NO,一种新型催化剂能使二者发生反应,生成两种常见的无毒气体”判断反应物、生成物、反应条件,再书写方程式.
(3)根据煤、煤气、液化石油气、天然气的特点及对环境的影响判断.
(4)根据碳元素守恒和天然气(主要成分是甲烷)和液化石油气(主要成分是丙烷和丁烷)中碳元素的质量分数判断燃烧产生二氧化碳的多少,得出天然气更环保的理由;根据甲烷的成分和燃烧的定义书写方程式;根据分子的性质和应用回答最后一问.
解答 解:(1)A、乙醇是植物的籽粒发酵蒸馏制成的,属于可再生性能源,所以正确;
B、乙醇和汽油都能燃烧放热,能用作汽车燃料,所以错误;
C、乙醇燃烧产生的空气污染物少,是一种清洁能源,使用乙醇汽油可减少大气污染,所以正确;
D、乙醇是可再生性能源,使用乙醇汽油可节省石油资源,所以正确.
(2)根据信息“汽车尾气中含有CO、NO,一种新型催化剂能使二者发生反应,生成两种常见的无毒气体”可知:反应物是CO、NO,反应条件是催化剂,根据生成物无毒及反应前后元素的种类不变,产物为二氧化碳和氮气,所以方程式为:2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2.
(3)煤是不可再生的,且燃烧会产生大量的空气污染物;煤气的主要成分是一氧化碳,有毒;液化石油气是石油产品,不可再生,燃烧也产生较多的空气污染物;天然气是较清洁的燃料;以上燃烧燃烧的主要产物都是二氧化碳.
A.以上燃烧燃烧的主要产物都是二氧化碳,不符合低碳经济原则,所以错误;
B.天然气是气体燃料,与空气接触面积大,燃烧的更充分,产生的大气污染物少,所以正确;
C.天然气属于化石燃料,是不可再生的能源,所以错误;
D、煤气、液化石油气、天然气相对于煤燃烧不讲,燃烧充分,含杂质少,燃烧产生的空气污染物少,所以正确.
(4)天然气和液化石油气中碳元素的质量分数分别约为75%和82.3%,则同质量的天然气和液化石油气中碳元素的质量天然气要少得多,根据碳元素守恒,它们燃烧生成的二氧化碳的质量天然气比液化石油气少,温室效应可减缓;燃烧是可燃物与氧气反应,条件是点燃,甲烷是由碳氢两种元素组成的,燃烧产物是二氧化碳和水,所以方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;分子之间有间隙,天然气减压后体积会膨胀,是因为减压后分子间的间隔变大.
答案:
(1)B;
(2)2CO+2NO$\frac{\underline{\;催化剂\;}}{\;}$N2+2CO2;
(3)B、D;
(4)充分燃烧等质量的天然气比液化石油气产生的二氧化碳少,可减缓温室效应(必须答与碳有关的理由).CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O; 分子间隔增大.
点评 能源与环境是人们关注的热点,也是考查的热点,使用乙醇汽油不但可以节省石油资源、有效地减少汽车尾气的污染,还可以促进农业生产.


科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Zn A Cu | B. | Zn Cu A | C. | A Zn Cu | D. | Cu A.Zn |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
 向盛有10g 氢氧化钠溶液(滴有2滴酚酞试液)的烧杯中滴入稀盐酸,恰好完全反应时消耗右图中稀盐酸的质量为10g,回答并计算:
向盛有10g 氢氧化钠溶液(滴有2滴酚酞试液)的烧杯中滴入稀盐酸,恰好完全反应时消耗右图中稀盐酸的质量为10g,回答并计算:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
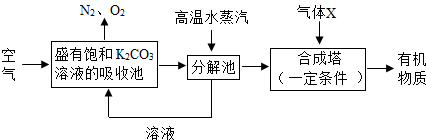
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com