
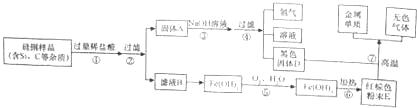
【题目】人们的日常生活离不开金属,高科技新材料的开发和应用也需要金属。硅钢可用于制造变压器的铁芯,某化学兴趣小组的同学为了验证硅钢(主要含有Fe、C、Si),设计了如图的实验流程(有些反应的部分反应物和生成物已省略)。
查阅资料发现:
常温下,单质硅(Si)不能与盐酸反应,但能与氢氧化钠溶液反应(Si+2NaOH+H2O═Na2SiO3+2H2↑)。
根据以上信息,回答下列问题:
(1)固体A的成分为 ,E的化学式为 。
(2)滤液B中的金属阳离子为 。
(3)在过滤操作时,若发现滤液浑浊,应 。
(4)步骤⑤中发生的是化合反应,尝试写出其化学方程式 。
【答案】
(1)碳、硅 Fe2O3;
(2)Fe2+
(3)查找原因,处理后重新过滤
(4)4Fe(OH)2+O2+2H2O=4Fe(OH)3
【解析】
试题分析:
(1)硅钢中的铁和盐酸反应会生成氯化亚铁和氢气,所以滤液B是氯化亚铁,固体A中含有碳、硅,硅和氢氧化钠溶液反应会生成硅酸钠和氢气,所以黑色固体D是碳,氢氧化铁加热生成氧化铁和水,所以E是氧化铁,氧化铁和碳在高温的条件下生成铁和二氧化碳,经过验证,推导正确,所以A是碳、硅,E的化学式为:Fe2O3;
(2)硅钢中主要含有Fe、C、Si,只有Fe能与稀盐酸反应生成氯化亚铁,所以剩余的固体A的成分中含有C、Si,滤液B中的金属阳离子为Fe2+;
(3)在过滤操作时,若发现滤液浑浊,应查找原因,处理后重新过滤;
(4)步骤⑤中发生的是化合反应中,反应物是Fe(OH)2与氧气和水,生成物是氢氧化铁,化学方程式是:4Fe(OH)2+O2+2H2O=4Fe(OH)3。


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:初中化学 来源: 题型:
【题目】黑豆是传统的养生食材,食用9°米醋泡制得到黑豆是一种很好的食疗方法.小明为判断家中的9°米醋含酸量是否合格,拟配制一定质量分数的氢氧化钠溶液进行测定.产品部分信息如图所示.请回答相关问题.

(1)配制100g质量分数为4%的氢氧化钠溶液需要水 mL(水的密度为1g/cm3).
(2)若9°米醋中的酸均看成是醋酸,醋酸与氢氧化钠反应的方程式为:
CH3COOH+NaOH═CH3COONa+H2O,小明取出10mL9°米醋,加入4%的氢氧化钠溶液12g,恰好完全反应.请通过计算判断该产品含酸量是否合格?(写出计算过程)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是甲、乙、丙三种物质的溶解度曲线,下列叙述正确的是 ( )

A. t1 ℃时,等质量的甲、丙溶液中所含溶质的质量分数为丙>甲
B. t2 ℃时,20 g丙溶解于50 g水中能形成70 g溶液
C. 分别将三种物质的饱和溶液从t3 ℃降温至t2 ℃时,所得溶液溶质质量分数的大小关系为乙>甲=丙
D. 若要将组成在N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能反映相关实验过程中量的变化的图象是( )

A. 用一氧化碳还原氧化铁
B. 等质量镁、锌分别和足量等质量分数的盐酸反应
C. 镁在氧气中燃烧
D. 等质量、等质量分数的双氧水完全分解
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类文明进步与金属材料的发展关系十分密切,金属在生活生产中有着非常广泛的应用。请回答下列问题:
(1)根据如图金属应用实例推断,金属具有的物理性质有 (至少答两点)。
(2)生铁和钢都是铁的合金,二者性能不同的原因是 。
(3)厨房中的下列物品所使用的主要材料属于金属材料的是 。
A、陶瓷碗 B、不锈钢炊具 C、橡胶手套 D、铜质水龙头
(4)微型化录音录像的高性能带中磁粉主要材料之一是化学组成相当于CoFe2O4的化合物,又知钴(Co)和铁都有+2、+3价,且在上述化合物中每种元素只具有一种化合价,则铁元素的化合价为 。
(5)某实验室废液中含有稀硫酸、硫酸亚铁和硫酸铜,若向其中加入一定量的锌,充分反应后过滤,向滤渣中加入盐酸,有气泡产生.则滤液中一定不含有的物质是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】实验与探究是化学学习的重要方法和内容,李明看到家里多年未用的铜制火锅上有绿色的锈迹,他对绿色锈迹的成分和性质产生了浓厚兴趣。
【查阅资料】
①绿色锈迹是碱式碳酸铜[Cu2(OH)2CO3],受热易分解;
②无水硫酸铜为白色粉末,遇水变蓝;
③碱石灰是CaO和NaOH的固体混合物,NaOH与CO2反应生成碳酸钠固体和水;
④氧化铜与稀硫酸反应生成蓝色溶液,碳粉不与稀硫酸反应也不溶解在稀硫酸中。
【发现问题】
查阅资料后,该同学将少量碱式碳酸铜放入试管中加热,发现试管中的固体由绿色变成黑色,同时试管壁上有无色液滴生成。
为了进一步确定碱式碳酸铜受热分解的产物,进行了如下探究:
探究一:碱式碳酸铜受热分解生成的黑色固体成分。
【猜想与假设】该黑色固体可能是①碳粉;② ;③碳和氧化铜的混合物。
【设计方案】请帮助该同学完成下述实验报告:
实验操作与现象 | 实验结论 |
猜想②正确 |
探究二:碱式碳酸铜受热分解还会生成CO2和H2O.
【进行实验】选择如下图所示装置进行验证:
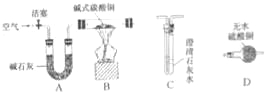
步骤一:连接A和B,打开活塞,通入一段时间的空气;
步骤二:点燃酒精灯,依次连接装置A→B→ → (填“C”,“D”);
步骤三:点燃酒精灯,观察到明显现象后,停止加热。
【解释与结论】
①当观察到 ,说明碱式碳酸铜受热分解生成了CO2和H2O,写出装置C中反应的化学方程式 ;
②写出Cu2(OH)2CO3受热分解的化学方程式 。
【反思与评价】
上述装置中A的作用是 。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】关于实验室电解水实验的说法不正确的是
A.实验室使用直流电对水进行电解
B.与电源正极相连的玻璃管内产生的气体可使带火星的木条复燃
C.电源正极与负极产生的气体质量比大约是1:2
D.电解时通常在水中加入少量稀硫酸溶液增强水的导电性
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验,向烧杯中的氢氧化钙溶液滴加一定量的稀盐酸后,发现忘记滴加指示剂,此时,他们停止滴加稀盐酸,并对烧杯内溶液中溶质的成分进行探究。
(1)写出该中和反应的化学方程式_______________________。
(2)探究烧杯内溶液中溶质的成分:
【作出猜想】 (A)溶质可能是CaCl2与Ca(OH)2 (B)可能是CaCl2
(C)溶质可能是CaCl2与HCl
【查阅资料】CaCl2溶液呈中性
【实验设计】
①取少量烧杯中的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色。于是排除了猜想(A),你认为排除猜想(A)的理由是_____________。
②小华想用碳酸钠溶液来验证后两种猜想,请你帮他完成实验,填写以下表格:
【交流反思】 为确定猜想(C)正确,下列几种实验方案不合理的是______(填字母)。
A.取反应后的溶液于试管中,滴加紫色石蕊试液变红色
B.取反应后的溶液于试管中,加入锌粉冒气泡
C.用洁净的玻璃棒蘸取反应后的溶液,涂抹在pH试纸上,测溶液的pH <7
D.取反应后的溶液于试管中,加入硝酸银溶液,生成白色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com