
草酸(H2C2O4)是一种有机物,在受热条件下分解生成水和另外二种氧化物。某校兴趣小组对此展开探究:
(1)常用 试剂检验生成物中是否含有水。
(2)对分解产物中的另外二种氧化物进行假设和验证:(图中固定试管的仪器已略去)
| 假设 | 实验 | 现象 | 结论 |
| 假设一: 生成物中有二氧化碳 | 将生成的气体通入澄清的石灰水 | 现象是 | 生成物中含有二氧化碳。 |
| 假设二: 生成物中有一氧化碳 | 用下图装置进行实验 | A中的现象是 | 生成物中含有一氧化碳。写出A中的反应化学方程式是 |
| 方案 | 步骤 | 不足 |
| 方案甲 | 先通一氧化碳,再点燃酒精灯 | |
| 方案乙 | 先点燃酒精灯,再通一氧化碳 | |

科目:初中化学 来源: 题型:探究题
学习氢氧化钠的性质之后,知道氢氧化钠溶液中含有H2O、Na+、OH-,能使无色酚酞溶液变红色,某科技小组想进一步探究是哪一种粒子使无色酚酞溶液变红色。
【提出猜想】猜想①:可能是H2O;
猜想②:可能是Na+;
猜想③:可能是OH-。
【实验验证】
| 实验操作 | 实验现象 | 结 论 |
| ①用试管取少量蒸馏水,滴入1滴~2滴无色酚酞溶液,振荡 | 试管内溶液仍为无色 | 水分子不能使无色酚酞溶液变红色 |
| ②用试管取少量氯化钠溶液,滴入1滴~2滴无色酚酞溶液,振荡 | | |
| ③用试管取少量氢氧化钠溶液,滴入1滴~2滴无色酚酞溶液,振荡 | | |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
氮气是一种重要的工业原料,广泛应用于化肥等工业。工业常用PSA变压吸附制氮气,某学习小组查阅到相关制氮气工艺流程,并展开学习,请回答相关问题:
【资料】:
1、碳分子筛对不同气体的吸附强度不同,如图所示;
2、气压越大,碳分子筛吸附能力越强,反之越弱;
3、碳分子筛可以再生,能重复使用。

(1)吸附塔中碳分子筛具有吸附性,这种性质是 (填“化学”、“物理”)性质,根据工艺流程,资料1图像中气体②是 (填化学式);
(2)根据资料,碳分子筛再生的方法是 。
(3)相比分离液态空气制氮气,该工艺的优点是 ;
(4)氮气可作食品保护气,是因为氮气化学性质 (填“稳定”、“活泼”)。N2和H2在500℃、200MPa及催化剂的条件下发生反应,生成NH3,反应的化学方程式为 ,反应中,N2和H2的质量比为 。
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
同学们为了研究氧化铁能否在氯酸钾制取氧气的实验中起催化作用,进行了以下实验:
【资料】①氯酸钾分解反应的化学方程式为 2KClO3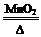 2KCl+3O2↑。
2KCl+3O2↑。
②氯酸钾和氯化钾均能溶于水。
【实验一】氧化铁能否在氯酸钾制取氧气实验中加快反应速率。
| 实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
| 1 | 0.6 | | 67 | 1800 |
| 2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
| 3 | 0.6 | g 氧化铁 | 67 | 89.5 |

| 装置 | 实验现象 | 实验分析 |
| A | 红色固体全部变黑 | 生成了铁 |
| B | 石灰水变浑浊 | 产生二氧化碳 |
| | 铁粉 | 氧化亚铁 | 氧化铁 | 四氧化三铁 |
| 颜色 | 黑色 | 黑色 | 红色 | 黑色 |
| 磁性 | 有 | 无 | 无 | 有 |
| 与CO反应 | 不反应 | 反应 | 反应 | 反应 |
| 与稀盐酸反应 | 反应 | 生成氯化亚铁和水 | 生成氯化铁和水 | 生成氯化亚铁、氯化铁和水 |
| 与硫酸铜溶液反应 | 反应 | 不反应 | 不反应 | 不反应 |
| 步骤 | 实验操作 | 实验现象 | 结论和解释 |
| 1 | 用磁铁吸引剩余固体 | _____________ | 剩余固体中没有氧化亚铁。 |
| 2 | __________________ | ______________ | 剩余固体中只有铁粉。 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
学校化学探究小组用HCl与大理石反应研究影响反应剧烈程度的因素。实验温度为25℃、35℃;大理石有细颗粒与粗颗粒两种规格,每次实验取用含碳酸钙60%的大理石10 g;所用HCl溶液的质量分数为9.125%、18.25%,每次实验HCl溶液的用量为20mL(假设两种溶液密度均为1 g/㎝3;大理石中杂质不与盐酸反应)。
【提出问题】:影响HCl与大理石反应的剧烈程度的因素有哪些?
【做出猜想】:
猜想一:大理石规格;猜想二:所用HCl溶液的质量分数;猜想三: 。
【实验探究】:完成以下实验设计方案并实验。
| 实验 编号 | T/℃ | 大理石 规格 | HCl的 质量分数 | 完全反应 的时间/s | 实验目的 |
| ① | 25 | 粗颗粒 | 18.25% | 160 | (I)实验①和②探究同体积下HCl质量分数对该反应剧烈程度的影响。 (II)实验①和③探究温度对该反应剧烈程度的影响。 (Ⅲ)实验①和④探究大理石规格对该反应剧烈程度的影响。 |
| ② | | | | 210 | |
| ③ | 35 | 粗颗粒 | 18.25% | 60 | |
| ④ | | | | 100 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
某校化学课外兴趣小组的同学在研究性学习课上展示了一套如下图所示的实验装置(假设每步化学反应都完全,氧化铁样品中的杂质不参加反应).
查阅资料:草酸在浓硫酸存在时加热发生如下反应:
H2C2O4 CO↑+CO2↑+H2O
CO↑+CO2↑+H2O
通过讨论,同学们对这套装置有了多种认识.
(1)第一小组同学说:从实验安全和实验操作程序看,首先要 ,实验开始先加热A处,实验结束时,应先停止D处的加热;从环境保护角度分析,此装置存在的明显不足是 ;
(2)第二小组的同学说:其中B装置的作用除去CO2;装置C的作用是 ;用该实验装置可以检验一氧化碳与氧化铁反应的产物,E装置的作用 ;一氧化碳与氧化铁反应的化学方程式为 .
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
科学家设想利用太阳能加热器“捕捉CO2”、“释放CO2”,实现碳循环(如下图所示)。
某化学小组的同学对此非常感兴趣,在老师的指导下,设计如下装置探究上述设想的反应原理。
(1)能证明“释放CO2”的现象是 。
(2)装置 B的作用是 。
(3)实验后小组同学对D中固体的成分进行探究。
【猜想与假设】D中的固体可能为①氧化钙;②氧化钙与碳酸钙; ③碳酸钙
【进行实验】甲同学取一定量的D中固体于试管中,并加入一定量的水,振荡,有白色不溶物,甲同学认为试管中的固体为碳酸钙,即猜想③成立。
乙同学认为上述实验不足以证明猜想③成立,其理由是 。他又重新进行实验,证明了猜想②成立,他的实验操作及现象为 。写出D中反应的化学方程式为 网]
(4)通过以上探究,小组同学认为科学家的设想在反应原理上是可行的。上述设想的优点有 (填字母序号).
A.原料易得
B.充分利用太阳能
C.释放出的CO2可作为重要资源加以利用
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
丽丽的爸爸旅游归来,带回一些钟乳硒石块送给了她.丽丽和同学们想验证钟乳石的主要成分是碳酸盐,于是她们将其中一块钟乳石带进实验室进行探究.
(1)请你帮助丽丽完成以下探究方案.
| 实验操作 | 预期的实验现象 | 实验结论 |
| ①取一小块钟乳石于试管中,向试管中加入 ,观察现象. ② ,观察现象. | 有气泡生成 | 钟乳石的主要成分是碳酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:探究题
当前市售珍珠粉的价格从五元到上百元不等,但其外观、手感都没有明显差异.
那么优质珍珠粉和廉价珍珠粉的成分有何不同呢?就此问题,实验小组同学展开探究.
【查找资料】
①优质珍珠粉直接由贝科动物体内珍珠加工而成,含有一定量的氨基酸、碳酸钙等.
②廉价珍珠粉由“贝壳粉”加工而成,贝壳加工过程中会用到氢氧化钠,贝壳的主要成分是碳酸钙.
③珍珠粉中除碳酸钙外,其它成分均不能与盐酸反应生成二氧化碳.
④氨基酸大部分能溶解于水,遇到浓硝酸并加热会呈现黄色或黑色.
⑤碳酸钙与浓硝酸能发生反应,生成二氧化碳.
⑥氯化钙溶液呈中性.
【提出猜想】
优质珍珠粉和廉价珍珠粉的区别可能在于:
①廉价珍珠粉含有 ;
②廉价珍珠粉不含氨基酸;
③碳酸钙含量不同.
【实验探究】
| 实验内容 | 现象 | 结论 |
| (1)分别将少量优质珍珠粉和廉价珍珠粉放入试管中,加少量水,静置一段时间后,滴加 . | 廉价珍珠粉的上层清液变红,优质珍珠粉的溶液没有变色 | 猜想①成立 |
| (2)分别将少量优质珍珠粉和廉价珍珠粉放入试管中,加少量水,加热. | 优质珍珠粉的溶液有黄色出现,局部变黑,廉价珍珠粉的溶液没有明显现象 | 猜想②成立 |
| | 优质珍珠粉 | 廉价珍珠粉 |
| 珍珠粉的质量 | 100 g | 100 g |
| 加入盐酸的质量 | 460.0 g | 501.3 g |
| 烧杯中最终物质的总质量 | 520.0 g | 557.7 g |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com