
我国化工专家侯德榜曾为世界制碱工业作出了突出贡献.“侯氏制碱法”是
食盐、氨气、二氧化碳等为原料先制得NaHCO3,进而生产出纯碱.其生产过程用化学方程式可简要表示为:
①NH3+CO2+H2O=NH4HCO3②NH4HCO3+NaCl=NaHCO3↓+NH4Cl
③2NaHCO3 Na2CO3+H2O+CO2↑ NH4HCO3
Na2CO3+H2O+CO2↑ NH4HCO3 NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑
(1)“侯氏制碱法”生产过程中没有涉及到的基本反应类型是 .
A.置换反应 B.化合反应 C.分解反应 D.复分解反应
(2)若第②步中得到的NaHCO3中含有少量的NH4HCO3.但不会影响产品Na2CO3的纯度,原因是 .
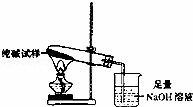
(3)若纯碱中含有NaHCO3杂质,为测定试样中纯碱的质量分数,用如图中的装置进行实验.主要实验步骤如下:用天平准确称量出干燥试管的质量为20.2克,然后称取4.0克已研碎的纯碱样品并放入干燥的试管中.用酒精灯加热,待充分反应并冷却后,在天平上称出试管和碳酸钠的质量23.5克.该试样中纯碱的质量分数为 .(保留一位小数)
| 纯碱的制取;反应类型的判定;根据化学反应方程式的计算.. | |
| 专题: | 常见的盐 化学肥料. |
| 分析: | (1)根据反应物、生成物的种类可以判断基本反应类型; (2)碳酸氢铵受热易分解; (3)利用酒精灯加热时,碳酸钠不能分解,碳酸氢钠分解生成碳酸钠、水和二氧化碳,反应前后的质量差即为反应生成水和二氧化碳的质量,根据水和二氧化碳的质量可以计算碳酸氢钠的质量,进一步可以计算该试样中纯碱的质量分数. |
| 解答: | 解:(1)①NH3+CO2+H2O=NH4HCO3中,反应物是三种,生成物是一种,属于化合反应; ②NH4HCO3+NaCl=NaHCO3↓+NH4Cl中,是两种化合物相互交换成分,生成另外两种新的化合物,属于复分解反应; ③2NaHCO3 由分析可知,“侯氏制碱法”生产过程中没有涉及到的基本反应类型是置换反应. 故填:A. (2)若第②步中得到的NaHCO3中含有少量的NH4HCO3.也不会影响产品Na2CO3的纯度,原因是碳酸氢铵受热易分解,生成氨气、水蒸气和二氧化碳,没有任何物质残留在碳酸钠中. 故填:碳酸氢铵受热易分解. (3)设碳酸氢钠的质量为x, 反应生成水和二氧化碳的质量为:20.2g+4.0g﹣23.5g=0.7g, 2NaHCO3 168 62 x 0.7g
x=1.9g, 该试样中纯碱的质量分数为: 答:该试样中纯碱的质量分数为52.5%. 故填:52.5%. |
| 点评: | 本题主要考查学生对反应类型的理解程度、运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性. |


科目:初中化学 来源: 题型:
下图所示的各物质中,E、F为具有香味的液态有机物。
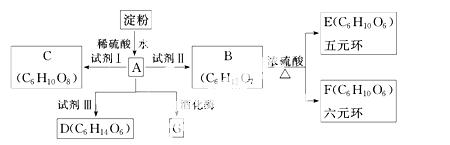
已知相关物质被氧化的顺序:RCHO>RCH2OH>RCHOHR1。
(1)B→E的反应类型是____________,F、C的结构简式分别为________________;E、F两种物质的关系是____________。
(2)试剂Ⅲ最可能是________,D的结构简式为_____________________________。
(3)下面对淀粉与A物质的有关描述中,正确的是________(填序号)。
a.均能发生水解反应
b.均属于糖类,且均有甜味
c.可用碘或银氨溶液作试剂将它们的溶液区别开
d.A脱水可得到淀粉
(4)1 mol D物质与足量B发生与B→E相同反应类型的反应时,最多能消耗________ mol B。
(5)写出有关反应的化学方程式:
A→B[试剂Ⅱ是新制Cu(O H)2悬浊液]: ___________________________________。
H)2悬浊液]: ___________________________________。
A→G:________________________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
实验室有一气体发生装置产生的无色气体可能含有H2、CO、CO2、HCl中的一种或几种,现将气体通过以下装置.

实验现象如下:B处由紫色变成红色;C处有白色沉淀生成;D处有白色沉淀生成;F处由黑色变成红色;G处由白色变成蓝色;H处无现象.
(1)无色气体肯定含 .
(2)由长颈漏斗加入的酸是 ,锥形瓶中装入的固体是少量 和 的混合物.
(3)E装置是为了排除对验证 的影响.
(4)E装置中浓硫酸(选填“能”或“不能”) 换成浓氢氧化钠.
(5)如果B装置中的试纸不变色,则可省去 、 装置(填装置代号).
查看答案和解析>>
科目:初中化学 来源: 题型:
已知氯磺酸化学式为ClSO3H,能在水中完全电离出H+和ClSO3﹣;甲酸化学式为HCOOH,能在水中部分电离出H+和HCOO﹣.对于反应C1SO3H+HCOOH═CO↑+HCl+H2SO4有如下判断,其中合理的是( )
|
| A. | 此反应属于复分解反应 | B. | 此反应中碳元素的化合价发生改变 |
|
| C. | 反应前后溶液的总质量不变 | D. | 反应后溶液的pH减小 |
查看答案和解析>>
科目:初中化学 来源: 题型:
将10克重的铁片浸入到硫酸铜溶液中,片刻后取出金属片,洗涤烘干,称得的固体质量为10.4克,则附在铁片上铜的质量为( )
|
| A. | 0.4克 | B. | 10.4克 | C. | 大于4克 | D. | 3.2克 |
查看答案和解析>>
科目:初中化学 来源: 题型:
工业烧碱具有较好的杀菌消毒作用且廉价易得,但工业烧碱中常含有杂质碳酸钠,某科学学习小组同学围绕工业烧碱样品纯度测定问题,展开了讨论与探究.

利用Na2CO3与稀H2SO4反应产生CO2,通过CO2质量的测定,确定样品中碳酸钠的质量,从而计算样品的纯度.
(1)小科同学根据以上思路,设计了如图甲的实验方案(固定装置省略),图中仪器A的名称是 .
(2)小明认为图甲实验方案的设计有缺陷,若按该方案进行测定会导致难以避免的误差,如装置内空气中的CO2没有排出、反应产生的CO2未被完全吸收等.为减小误差,使CO2质量的测定更准确,该小组同学根据以上讨论,对图甲方案进行改进,设计了如图乙的实验方案(固定装置省略).
图乙B装置中样品在与稀硫酸反应前和停止反应后,都要通过量的空气,反应前通空气时a、b、c三个弹簧夹的开闭情况是 .
(3)若撤去图乙中的C装置,则测得工业烧碱的纯度将 (填“偏高”“偏低”或“无影响”).
(4)已知:碳酸钠溶液与稀硫酸反应先生成碳酸氢钠,当碳酸钠全部转变为碳酸氢钠后,生成的碳酸氢钠能继续与稀硫酸反应生成二氧化碳.现向纯碱样品中加一定量的稀硫酸,反应后产生无色气体并得到X溶液.请分析推断反应后所得X溶液的溶质,其所有的可能组成为 .
查看答案和解析>>
科目:初中化学 来源: 题型:
分类是学化学的方法之一,下列物质是按氧化物、盐、混合物顺序排列的是( ▲ )
A、蒸馏水、大理石、澄清石灰水 B、酒精、硫酸钠、泥浆水
C、氧化铜、高锰酸钾、冰水混合物 D、干冰、碳酸钙、空气
查看答案和解析>>
科目:初中化学 来源: 题型:
下列各组中,物质的俗称、学名与化学式表示同一物质的是( )
|
| A. | 纯碱 氢氧化钠 NaOH | B. | 生石灰 氧化钙 CaO |
|
| C. | 胆矾 硫酸铜 CuSO4 | D. | 干冰 水 H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:
区别下列各组物质,选用的方法或试剂不正确的是( )
| 物 质 | 选用的方法或试剂 | |
| A | 二氧化碳和氮气 | 燃着的木条 |
| B | 二氧化锰和食盐 | 观看颜色 |
| C | 氧气和二氧化硫 | 闻气味 |
| D | | 点燃观察现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com