
| 序号 | 化学反应事实 | 影响反应的因素 |
| A | 二氧化碳常温下与水反应,生成碳酸,光合作用时则生成葡萄糖 | 反应条件 |
| B | 碳在常温下不与氧气反应,而在点燃时能与氧气反应 | 反应温度 |
| C | 双氧水在常温下较难分解,而在加入二氧化锰后迅速分解 | 催化剂 |
| D | 铜片在空气中很难燃烧,铜粉在空气中较易燃烧 | 反应物的种类 |
| A. | A | B. | B | C. | C | D. | D |
分析 影响化学反应的因素有:温度,温度越高,反应越快;反应物的接触面积,物质间的接触面积越充分,反应速度越快;反应物颗粒的大小,颗粒越小,反应速度越快;通常反应物的浓度越大,反应速度越快;加入催化剂可以改变其反应速率等;据此结合事实进行分析解答.
解答 解:A、二氧化碳常温下与水反应,生成碳酸,光合作用时则生成葡萄糖,说明反应条件不同,生成物不同,故选项推理合理.
B、碳在常温下不与氧气反应,而在点燃时能与氧气反应,说明反应的温度影响化学反应的发生,故选项推理合理.
C、双氧水在常温下较难分解,而在加入二氧化锰后迅速分解,说明了使用催化剂,可以改变化学反应的速率,故选项推理合理.
D、铜片在空气中很难燃烧,铜粉在空气中较易燃烧,说明反应物表面积,可以影响化学反应;铜粉与铜片是同一种物质,不能说明反应物种类影响化学反应的进行,故选项推理不合理.
故选:D.
点评 本题难度不是很大,了解影响反应的因素即可正确解答本题,可从温度、反应物的接触面积,反应物颗粒的大小、反应物的浓度及催化剂等方面进行分析考虑.


科目:初中化学 来源: 题型:多选题
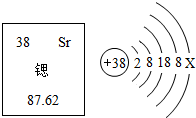 锶元素在元素周期表中的信息与锶原子结构示意图如图所示,下列说法错误的是( )
锶元素在元素周期表中的信息与锶原子结构示意图如图所示,下列说法错误的是( )| A. | Sr为金属元素 | B. | 乙图中X≡3 | ||
| C. | 锶原子的质量为87.62g | D. | 锶原子的质子数是38 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
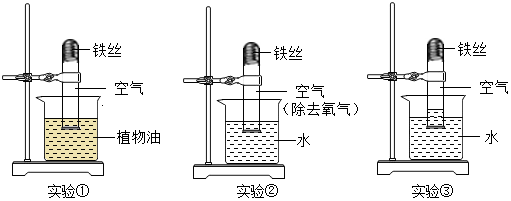
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 同时生成D的质量是9克 | |
| B. | B与D的相对分子质量之比是8:1 | |
| C. | 参加反应的A与生成C的质量之比是8:11 | |
| D. | 若A的相对分子质量是32,则C的相对分子质量是44 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.
某兴趣小组为验证质量守恒定律,做了镁条在空气中燃烧的实验.| 操作步骤 | 实验现象 | 实验结论 |
| 取少量黄色固体于试管中,加入适量的水,并将湿润的红色石蕊试纸放在试管口 | 试管中有气体产生,湿润的红色石蕊试纸变蓝 | 黄色固体为Mg3N2 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
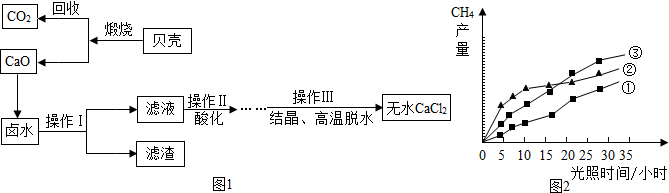
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
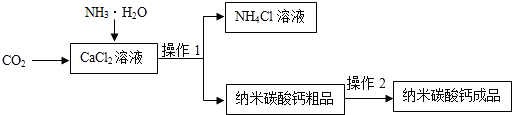
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com