
含8克NaOH的溶液中通入一定量的H2S气体后,可发生以下反应:NaOH+H2S=NaHS+H2O,2NaOH+H2S=Na2S+2H2O,将得到的溶液小心蒸干,称得无水固体7.9g,则该固体中一定含有的物质是( )
A.Na2S B.NaHS C.Na2S和NaHS D.Na2S和NaOH
【考点】根据化学反应方程式的计算.
【专题】混合物组成的判断.
【分析】(1)注意反应顺序:NaOH先和H2S反应生成NaHS,若NaOH还有剩余,则NaOH继续和NaHS反应生成Na2S;
(2)反应产物分三种情况进行讨论:
①NaOH少量,产物只有NaHS;
②NaOH和H2S反应生成NaHS后还有剩余,产物是NaHS和Na2S的混合物;
③NaOH和NaHS反应完后还过量,产物是NaOH和Na2S的混合物.
(3)利用极值法判断产物的类型.
【解答】解:①若NaOH少量,则产物只有NaHS,那么固体质量应该增加,而实际固体质量在减小,因此不可能是NaOH少量;
②若NaOH和H2S反应产物为NaHS和Na2S的混合物,则根据极值法进行判断,
若产物只有NaHS,设8克NaOH反应可生成硫氢化钠的质量为x,
NaOH+H2S=NaHS+H2O
40 56
8g x
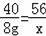

x=11.2g
若产物只有Na2S,设8克NaOH反应可生成硫化钠的质量为y,
2NaOH+H2S=Na2S+2H2O
80 78
8g y


y=7.8g
而实际称得无水固体7.9g,7.8g<7.9g<11.2g,因此生成物可能是NaHS和Na2S的混合物.
③若NaOH过量,则产物为NaOH和Na2S的混合物,则生成固体质量应该介于7.8g和8.0g之间,而实际称得无水固体7.9g,因此固体混合物也可能是NaOH和Na2S的混合物.
综上所得,固体中一定含有的物质是Na2S.
故选A.
【点评】利用假设法或极限法,便于学生理解和掌握,考查了学生利用化学反应方程式进行计算的能力,提高了学生分析问题的能力.


科目:初中化学 来源: 题型:
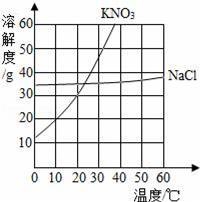
如图为硝酸钾和氯化钠的溶解度曲线.由图可知:
(1)当温度为10℃时,硝酸钾的溶解度 (填“>”、“<”或“=”)氯化钠的溶解度.
(2)欲使饱和的硝酸钾溶液变为不饱和溶液,可以采取的方法是 (写一种方法即可)
(3)当氯化钠中含有少量硝酸钾时,可用 法提纯氯化钠.
(4)氯化钠属于 (填“易溶”“可溶”“微溶”或“难溶”)物质.

查看答案和解析>>
科目:初中化学 来源: 题型:
小婧做探究性实验:用称量法测定铁在O2中燃烧的产物.发现5.6g铁在足量的O2中燃烧得到7.82g固体.小婧排除了其他因素可能产生的误差,则她得到的固体产物可能是( )
A.Fe3O4和Fe的混合物 B.Fe3O4和FeO的混合物
C.Fe3O4、FeO和Fe的混合物 D.Fe3O4和Fe2O3的混合物
查看答案和解析>>
科目:初中化学 来源: 题型:
铝镁合金因密度小、强度高、刚性好等特点,在人类生活中应用广泛.某兴趣小组的同学对编号为①、②的两种铝镁合金样品进行了如下实验.
已知:镁能与酸反应,但不能与碱溶液反应;铝既能与酸反应,又能与氢氧化钠等碱溶液反应,化学方程式为:2Al+2NaOH+2H2O═2NaAlO2+3H2↑,NaAlO2溶液与二氧化碳反应能产生氢氧化铝沉淀,后者经过滤、洗涤、灼烧后生成相应氧化物.
(1)取质量为m的样品①和过量的氢氧化钠溶液反应,然后过滤;再向滤液中通入过量的二氧化碳气体,将所得沉淀过滤、洗涤、烘干、灼烧,所得固体的质量仍为m.求样品①中铝的质量分数.
(2)取不同质量的样品②分别和30 g相同浓度的盐酸反应,所取合金质量与产生气体体积(气体的密度为0.089 3 g/L)如表所示:
| 实验序号 | a | b | c |
| 合金质量/mg | 510 | 765 | 918 |
| 气体体积/mL | 560 | 672 | 672 |
求:合金中铝镁的质量比.
查看答案和解析>>
科目:初中化学 来源: 题型:
在相同条件下,H2S(氢硫酸)的酸性比H2SO3(亚硫酸)的酸性强,H2S(氢硫酸)是H2S(硫化氢)气体的水溶液,H2SO3(亚硫酸)是SO2与水反应后形成的溶液.在室温时,向饱和的H2SO3溶液中通入H2S气体,发生反应如下:2H2S+H2SO3═3S↓+3H2O.以下是向H2SO3溶液通入H2S的体积和溶液pH值关系图,正确的是( )
A.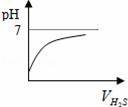
 B.
B.

C.
 D.
D.

查看答案和解析>>
科目:初中化学 来源: 题型:
社会实践活动中,课外兴趣小组对某钢铁厂的铁矿石样品和钢样进行实验、分析、计算,了解了该钢铁厂生产原料、产品的相关信息.下面请你根据他们的实验帮助计算回答:
取该厂的某钢样粉末28.36g(假设只含Fe和C),在氧气流中充分反应,将产生的气体通入足量的澄清石灰水中,得到3g白色沉淀.
(1)计算此钢样粉末中铁和碳的质量之比.
(2)再取三份不同质量的钢样粉末分别加到50g质量分数相同的硫酸中,充分反应后,测得的实验数据如下表所示:(标准状况下,2g H2的体积为22.4 L)
| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| 加入钢样粉末的质量/g | 2.836 | 5.672 | 8.508 |
| 生成气体的体积(标准状况)/L | 1.12 | 2.24 | 2.80 |
请根据表中数据计算硫酸中H2SO4的质量分数.
(3)若在实验Ⅱ中继续加入m g钢样粉末,计算反应结束后剩余的固体质量为多少?(用含m的代数式表示)
查看答案和解析>>
科目:初中化学 来源: 题型:
据报,2014年6月2日,瑞士帕耶讷,全球最大的太阳能飞机“阳光动力2号”首飞.据报道,这架飞机机翼上安装有1.7万块超薄且高效能的太阳能电池板,翼展长达72米.太阳能板在日间吸收能量,让飞机在晚间也可飞行,飞行时间不再受燃油量限制.请回答下列问题:
(1)制成该飞机的机体材料可以是 ;(在A.B、C中选填)
A.韧性好、硬度大的锰钢
B.强度好、密度小的铝合金
C.抗腐蚀性好的不锈钢
(2)太阳能飞机工作过程中的能量转化是从 能开始,最终转化为 能.
(3)硅是太阳能电池中不可缺少的材料,硅生产过程中的一个重要化学反应为:在高温条件下,利用单质碳还原二氧化硅,同时生成一种可燃性气体.则发生化学反应的方程式是 ,该反应前后硅元素的化合价分别为 .


查看答案和解析>>
科目:初中化学 来源: 题型:
实验室里取8mL水并进行加热,下列需用的化学仪器组合正确的是( )
①带铁夹的铁架台;②10mL量筒;③100mL量筒;④酒精灯;⑤石棉网;⑥试管;⑦试管夹;⑧胶头滴管.
A.②④⑥⑦ B.①③④⑥⑧ C.①②④⑥⑧ D.①②④⑤⑥
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com