

| 溶质质量 |
| 溶液质量 |
| 60g |
| 60g+100g |


科目:初中化学 来源: 题型:
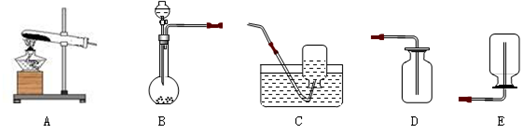
查看答案和解析>>
科目:初中化学 来源: 题型:
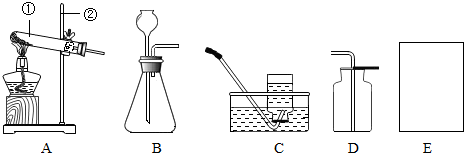
| 实验序号 | 过氧化氢溶液浓度∕% | 过氧化氢溶液体积∕mL | 温度∕℃ | 二氧化锰用量∕g | 收集氧气体积∕mL | 反应所需时间∕s |
| A | 5 | 1 | 20 | 0.1 | 4 | 16.75 |
| B | 15 | 1 | 20 | 0.1 | 4 | 6.04 |
| C | 30 | 5 | 35 | ∕ | 2 | 49.21 |
| D | 30 | 5 | 55 | ∕ | 2 | 10.76 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| 实 验 操 作 | 实 验 目 的 |
| 1、给试管中的固体加热应先预热 | 防止受热不均匀 |
| 2、排水法收集完氧气后,先从水槽中移出导管后熄灭酒精灯 | |
| 3、 |
|
| 4、 |
|
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com