
分析 (1)根据混合溶液的质量为废水和酸的质量之和来计算;
(2)利用酸碱反应的化学方程式,将硫酸质量代入方程式计算氢氧化钠的质量,再计算废水中氢氧化钠的质量分数;
(3)利用氢氧化钠的质量利用反应的化学方程式,求出可获得硫酸钠的质量.
解答 解:(1)反应后的质量为61.1g,反应前的质量为41.5g,
则10%的硫酸溶液的质量为61.1g-41.5g=19.6g,
(2)硫酸的质量为19.6g×10%=1.96g,
设废水中氢氧化钠的质量为x,
则2NaOH+H2SO4═Na2SO4+2H2O
80 98
x 1.96g
$\frac{80}{x}=\frac{98}{1.96g}$
x=1.6g
废水样品中烧碱的质量分数=$\frac{1.6g}{41.5g-25.5g}×$100%=10%
(3)设每天可获得硫酸钠的质量为y
2NaOH+H2SO4═Na2SO4+2H2O
80 142
32t×10% y
$\frac{80}{32t×10%}=\frac{142}{y}$
y=5.68t
答案:
(1)19.6
(2)该废水样品中烧碱的质量分数为10%
(3)5.68t
点评 本题考查废水中氢氧化钠的质量分数的计算,计算硫酸的质量是关键,然后将硫酸质量代入化学反应方程式计算即可解答.


 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案科目:初中化学 来源: 题型:选择题
| A. | 铝锭难被压缩,因为铝原子间没有间隙 | |
| B. | 若家中燃气泄漏,应立即打开排气扇或抽油烟机 | |
| C. | pH大于5.6的雨水为酸雨,能使紫色石蕊溶液变红 | |
| D. | 生活中为了降低水的硬度往往采用加热煮沸 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 硝酸钾的溶解度变大 | B. | 溶质的质量分数保持不变 | ||
| C. | 所的溶液的质量为120g | D. | 所得溶液是饱和溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 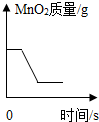 加热氯酸钾和二氧化锰的混合物 | |
| B. | 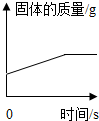 向一定量的铁粉中加入硫酸铜溶液 | |
| C. | 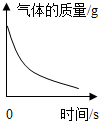 加热一定量的碳酸氢铵固体 | |
| D. | 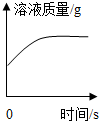 向某温度的硝酸钾饱和溶液中加入硝酸钾晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
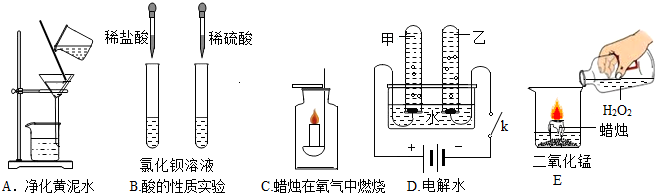
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Fe2O3中铁元素质量分数为70% | B. | 该反应属于放热反应 | ||
| C. | 反应前后铁元素的质量不变 | D. | SO2中硫、氧元素的个数比为1:2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com