
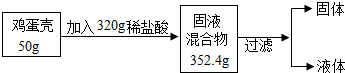
 已知鸡蛋壳的主要成分是碳酸钠(其他成分不与水也不与盐酸反应),某课外活动兴趣小组的同学为了测定鸡蛋壳中碳酸钙的含量,进行如下实验:
已知鸡蛋壳的主要成分是碳酸钠(其他成分不与水也不与盐酸反应),某课外活动兴趣小组的同学为了测定鸡蛋壳中碳酸钙的含量,进行如下实验:分析 (1)根据质量守恒定律计算生成二氧化碳的质量;
(2)根据二氧化碳的质量和化学方程式计算参加反应的碳酸钙质量,然后计算碳酸钙的质量分数.
解答 解:(1)生成二氧化碳的质量为:50g+320g-352.4g=17.6g;
(2)设鸡蛋壳中碳酸钙的质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 17.6g
$\frac{100}{x}$=$\frac{44}{17.6g}$
x=40g
所以碳酸钙的质量分数为:$\frac{40g}{50g}$×100%=80%.
答:鸡蛋壳中碳酸钙的质量分数为80%.
点评 本题主要考查了化学方程式的计算,难度不大,注意解题的规范性.


 周周清检测系列答案
周周清检测系列答案 轻巧夺冠周测月考直通高考系列答案
轻巧夺冠周测月考直通高考系列答案科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
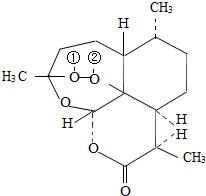 中国科学家屠呦呦因发现抗疟疾中药青蒿素而获得诺贝尔生理或医学奖.青蒿素化学式为C15H22O5,下列有关说法正确的是( )
中国科学家屠呦呦因发现抗疟疾中药青蒿素而获得诺贝尔生理或医学奖.青蒿素化学式为C15H22O5,下列有关说法正确的是( )| A. | 青蒿素由碳、氢、氧三种原子构成 | |
| B. | 青蒿素中碳、氢、氧三种元素的质量比为15:22:5 | |
| C. | 青蒿素是一种有机物 | |
| D. | 青蒿素的相对分子质量为282g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com