
| A、使CO2更易被吸收 | B、NH3比CO2更易制取 | C、CO2的密度比NH3大 | D、为了增大NaHCO3的溶解度 |
科目:初中化学 来源: 题型:
| A、图书馆资料着火时,用泡沫灭火器灭火 | B、炉子上只要放一壶水,就能防止煤气中毒 | C、禁止使用含硫高的劣质煤,可减少二氧化硫对空气造成的污染 | D、厨房里液化气泄漏时,立刻打开排风扇 |
查看答案和解析>>
科目:初中化学 来源: 题型:
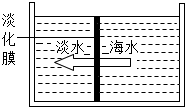 海洋是巨大的资源宝库,请你运用学过的知识回答下列问题:
海洋是巨大的资源宝库,请你运用学过的知识回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:
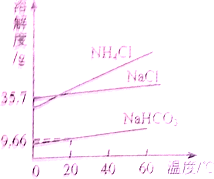 实验室模拟“侯氏制碱法”制纯碱,其原理是NaCl+NH4HCO3=NaHCO3+NH4Cl,再将碳酸氢钠加热分解得到纯碱.如图是NaCl、NH4Cl、NaHCO3的溶解度曲线,下列说法正确的是( )
实验室模拟“侯氏制碱法”制纯碱,其原理是NaCl+NH4HCO3=NaHCO3+NH4Cl,再将碳酸氢钠加热分解得到纯碱.如图是NaCl、NH4Cl、NaHCO3的溶解度曲线,下列说法正确的是( )| A、NaHCO3从溶液中分离出,可采用的操作是蒸发结晶 | B、NH4Cl饱和溶液的溶质质量分数一定大于NaCl饱和溶液的溶质质量分数 | C、40℃时,溶解度大小关系是:NH4Cl>NaCl>NaHCO3 | D、20℃时,100g水中加入11.7g NaCl和15.8g NH4HCO3固体,充分反应后,理论上可析出7.14g NaHCO3晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:

| ||
| 物质 | NaCl | NaHCO3 | NH4Cl | NH3 | CO2 |
| 溶解度 | 36.0g | 9.6g | 37.2g | 710 | 0.9 |
| 工业纯碱标准:(Na2CO3%≥) | ||
| 优等品 | 一等品 | 合格品 |
| 99.2 | 98.8 | 98.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:
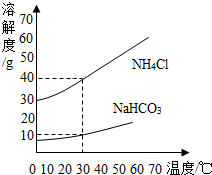 1926年,我国著名化学家侯德榜先生创立了一种高效环保的纯碱生产方法--“联合制碱法”,又称侯氏制碱法.其生产过程中有下列反应:
1926年,我国著名化学家侯德榜先生创立了一种高效环保的纯碱生产方法--“联合制碱法”,又称侯氏制碱法.其生产过程中有下列反应:
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、有机物中都含有碳元素,含碳元素的物质都是有机物 | B、各种酸溶液中都含有氢离子(H+),使酸溶液具有许多共同的性质 | C、化合物含有不同种元素,含有不同种元素的物质一定是化合物 | D、溶液的特性告诉我们,只要是均一、稳定的液体就是溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com