
| A. | 制取CO2气体时,始终收集不到CO2-收集CO2的集气瓶没盖严 | |
| B. | 点燃氢气时,发生爆炸-点燃前可能没有检验氢气的纯度 | |
| C. | 细铁丝在氧气中燃烧时,集气瓶底炸裂-用于引燃的火柴过长 | |
| D. | 验证空气中氧气含量时,进入集气瓶中的水少于$\frac{1}{5}$-红磷过量 |
分析 A、始终收集不到气体,可能是由于装置漏气所引起,集气瓶没盖严不会影响二氧化碳的收集;
B、氢气具有可燃性,可燃性气体与空气混合点燃时可能会发生爆炸,因此在点燃可燃性气体前一定要检验气体的纯度;
C、铁丝燃烧放出大量的热,反应后的高温生成物若直接溅落在集气瓶底,瓶底会炸裂;而引燃火柴过长则可能造成铁丝不能燃烧;
D、验证空气中氧气含量时,为使氧气完全反应,需要加入过量的红磷;而进入水的量少于五分之一则可能是由于红磷量不足所造成.
解答 解:A、制取二氧化碳时,始终收集不到气体,可能是由于装置漏气所引起;而收集时集气瓶没盖严并不影响气体的收集,故错误;
B、可燃性气体氢气点燃时发生爆炸,可推断氢气不纯、在点燃氢气前没有进行纯度的检查,故正确;
C、细铁丝在氧气中燃烧时,为了防止高温生成物直接落在瓶底而使瓶底炸裂,而在集气瓶底放少量水或铺一层沙;故集气瓶底炸裂,可能是由于集气瓶底没留水或未铺沙,与引燃火柴过长无关,引燃火柴过长只会造成氧气的大量消耗,造成铁丝不能燃烧,故错误;
D、测定氧气的含量时,验证空气中进入水的量不足五分之一,可能是由于红磷量不足氧气未能完全消耗所造成的,故错误;
故选B.
点评 常见的实验现象的分析方法:收集与此有关的资料,对能够引起异常现象原因作出假设,然后判断所给的信息是不是可能引起这样异常现象.


科目:初中化学 来源:2017届湖北省九年级下学期第二次月考化学试卷(解析版) 题型:选择题
下列物质按单质、氧化物、化合物、混合物的顺序排列的是( )
A.金刚石、生石灰、粗食盐、冰水
B.水银、干冰、熟石灰、天然气
C.苛性钠、铁锈、纯碱、石油
D.硫磺、液态氧、粗食盐、胆矾
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源:2017届江苏省苏州市区九年级一模调研测试化学试卷(解析版) 题型:选择填充题
下列各组物质在pH=0的溶液中能大量共存,且能形成无色溶液的是
A. Na2SO4、KCl、Na2CO3 B. NaNO3、K2SO4、CuCl2
C. BaCl2、Na2SO4、KOH D. KNO3、HCl、Na2SO4
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
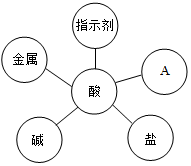 构建知识网络是学习化学的重要方法之一.某同学在学习酸、碱和盐的化学性质后,归纳的知识网络如图,图中“-”两端的物质可以反应.请帮助该同学进行完善和纠正.
构建知识网络是学习化学的重要方法之一.某同学在学习酸、碱和盐的化学性质后,归纳的知识网络如图,图中“-”两端的物质可以反应.请帮助该同学进行完善和纠正.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | NH4+、Na+、NO3- | B. | H+、Ca2+、CO32- | C. | Ba2+、OH-、SO42- | D. | K+、Na+、MnO4- |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
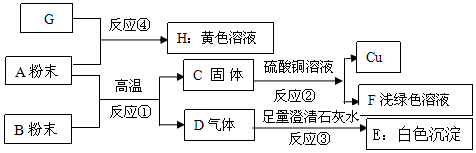
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 交通是城市发展的重要标志.请回答下列问题:
交通是城市发展的重要标志.请回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com