
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
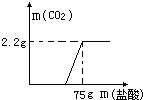 某化学兴趣小组对实验室留置的NaOH的变质程度进行探究.先称取13.3gNaOH样品(杂质为Na2CO3 ),配制成50g溶液,然后向溶液中逐滴加入质量分数为14.6%稀盐酸,实验测得加入稀盐酸的质量与产生CO2 气体的质量关系如图.试计算:
某化学兴趣小组对实验室留置的NaOH的变质程度进行探究.先称取13.3gNaOH样品(杂质为Na2CO3 ),配制成50g溶液,然后向溶液中逐滴加入质量分数为14.6%稀盐酸,实验测得加入稀盐酸的质量与产生CO2 气体的质量关系如图.试计算:查看答案和解析>>
科目:初中化学 来源: 题型:
 实验室有失去标签的两瓶白色粉末药品,分别是Na2CO3和NaHCO3.某同学设计了下列实验进行鉴别,如图所示.
实验室有失去标签的两瓶白色粉末药品,分别是Na2CO3和NaHCO3.某同学设计了下列实验进行鉴别,如图所示.| 步骤 | 实验操作 |
| 1 | 往两个相同的锥形瓶中分别加入50g溶质质量分数为14.6%的稀盐酸 |
| 2 | 用相同两只气球,分别装入足量的两瓶中的白色粉末各20g,套在步骤1的锥形瓶口,如图 |
| 3 | 迅速将气球中的药品,倒入锥形瓶中 |
查看答案和解析>>
科目:初中化学 来源:轻巧夺冠优化训练·人教版·九年级化学下 题型:038
向
50g质量分数为14.6%的盐酸中,加入一定量20%的烧碱溶液恰好完全反应,求所得溶液中溶质的质量分数.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com