
25 ℃时,pH=3的盐酸a L分别与下列三种溶液充分混合后,溶液均呈中性:①c(NH3·H2O)=10-3 mol·L-1的氨水b L,②c(OH-)=10-3 mol·L-1的氨水c L,③c(OH-)=10-3 mol·L-1的Ba(OH)2溶液d L。试判断a、b、c、d的数量大小关系为( )
A.a=b>c>d B.b>a=d>c C.b>a>d>c D.c>a=d>b
科目:初中化学 来源: 题型:
轻轨电车是近年来城市发展中的一种无污染的新兴交通工具,当轻轨电车开动时,轻轨电车与架空电线的接触点由于高速摩擦会产生高温,因此接触点上的材料应该具有耐高温,不易氧化、能导电的性质,你认为接触点上的材料应选用
A.金刚石 B.铝 C.石墨 D.铜
查看答案和解析>>
科目:初中化学 来源: 题型:
小林同学用相同的铁钉探究铁生锈与哪些因素有关,设计的实验如右图。经过一周观察:试管A 和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀。根据上述描述请你完成:
 (1)铁生锈是铁与 和 同时接触并发生化学反应形成的,铁锈的主要成分化学式为___________;
(1)铁生锈是铁与 和 同时接触并发生化学反应形成的,铁锈的主要成分化学式为___________;
(2)A中的蒸馏水事先要煮沸,其目的是 ,C中干燥剂的作用是 ;
(3)要防止铁器生锈通常有多种措施,不同的铁制品所采取的防锈措施有所不同。如自行车的链条常采用 的方法防锈,自行车的支架常采用 的方法防锈;
(4)以下措施不能阻止铁器生锈的 是(填序号) 。
是(填序号) 。
①喷漆、②刷搪瓷漆、③水洗、④镀一层耐腐蚀金属。
查看答案和解析>>
科目:初中化学 来源: 题型:
市售过碳酸钠(Na2CO4)中往往含有少量杂质碳酸钠,化学兴趣小组同学购得一包市售过碳酸钠样品,欲测定样品中过碳酸钠的质量分数:
【阅读资料】
①过碳酸钠和盐酸反应的化学方程式为2Na2CO4+4HCl=4NaCl+2CO2↑+O2↑+2H2O
②常温常压下,氧气的密度为1.429g/L
③过碳酸钠通常用作洗衣粉的助剂,可以去除多种顽固污渍,同时清除细菌和异味。
【讨论探究】
甲同学认为可以通过测定反应生成的二氧化碳的体积,求得样品中过碳酸钠的质量分数;乙同学认为可以通过测定反应生成的氧气的体积,求得样品中过碳酸钠的质量分数。兴趣小组经过讨论后,认为甲同学的方案不合理。请你写出可能的原因 ________
_____________________________________________________________________________。
【定量测定】
同学们根据乙同学的实验方案,设计了实验装置(如下图所示),取8.0 g样品投入烧瓶中,逐滴滴加盐酸直至不再产生气泡为止。

(1)装置B的作用是_______________________________________________。
(2)装置C的作用是_______________________________________________。
(3)通过排水量测定氧气的体积为672.0 mL,请计算样品中过碳酸钠的质量分数是多少?
(最后得数保留小数点后一位)
查看答案和解析>>
科目:初中化学 来源: 题型:
下列叙述正确的是( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2 mol·L-1的盐酸与等体积水混合后pH=1
D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目:初中化学 来源: 题型:
将0.2 mol·L-1 HA溶液与0.2 mol·L-1 NaOH溶液等体积混合,测得混合溶液中c(Na+)>c(A-),则(用“>”、“<”或“=”填写下列空白):
(1)混合溶液中c(HA)________c(A-);
(2)混合溶液中c(HA)+c(A-)________0.1 mol·L-1;
(3)混合溶液中由水电离出的c(OH-)______0.2 mol·L-1 HA溶液中由水电离出的c(H+);
(4)25℃时,如果取0.2 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合,测得混合溶液的pH<7,则HA的电离程度________NaA的水解程度。
查看答案和解析>>
科目:初中化学 来源: 题型:
已知反应:①101 kPa时,C(s)+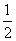 O2(g)===CO(g) ΔH1=-110.5 kJ·mol-1
O2(g)===CO(g) ΔH1=-110.5 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq)===H2O(l) ΔH2=-57.3 kJ·mol-1
下列结论正确的是( )
A.若碳的燃烧热用ΔH3来表示,则ΔH3<ΔH1
B.若碳的燃烧热用ΔH3来表示,则ΔH3>ΔH1
C.浓硫酸与稀NaOH溶液反应的中和热为57.3 kJ·mol-1
D.稀醋酸与稀NaOH溶液反应生成1 mol水,放出的热量为57.3 kJ
查看答案和解析>>
科目:初中化学 来源: 题型:
已知甲为恒温、恒压容器,乙为恒温、恒容容器。两容器中均充入1 mol N2、3 mol H2,初始时两容器的温度、体积相同。一段时间后反应达到平衡,为使两容器中的N2在平衡混合物中的物质的量分数相同,下列措施中可行的是( )
A.向甲容器中充入一定量的氦气
B.向乙容器中充入一定量的N2
C.升高乙容器的温度
D.增大甲容器的压强
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com