
| A. | 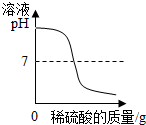 向一定量的氢氧化钠溶液中滴加稀硫酸至过量 | |
| B. | 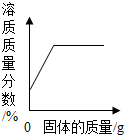 在一定温度下,向饱和的硝酸钾溶液中不断加入硝酸钾固体,充分搅拌 | |
| C. |  等质量的锌粉和铁粉与足量的稀硫酸反应 | |
| D. | 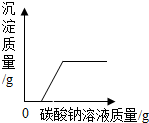 向含有HCl和CaCl2的混合溶液中加入Na2CO3溶液 |
分析 A、向氢氧化钠溶液中不断滴加稀盐酸液,氢氧化钠与盐酸反应生成氯化钠和水,随着反应的进行,碱性逐渐变弱,恰好完全反应时显中性,继续加入稀盐酸液,溶液显酸性,据此进行分析判断.
B、在一定温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体,硝酸钾晶体继续溶解至饱和,溶液的溶质质量变大,达饱和后硝酸钾不再溶解,溶液的质量分数不再改变;据此进行分析判断.
C、锌比铁活泼,与盐酸反应速度锌大于铁;等质量的铁生成是氢气要比锌生成的氢气多.
D、向HCl和CaCl2的混合溶液中加入Na2CO3溶液时,Na2CO3溶液先与盐酸反应生成氯化钠、水和二氧化碳,开始时不会生成沉淀,盐酸消耗完再与CaCl2
解答 解:
A、向氢氧化钠溶液中不断滴加稀盐酸液,氢氧化钠与盐酸反应生成氯化钠和水,随着反应的进行,碱性逐渐变弱,恰好完全反应时显中性,继续加入稀盐酸液,溶液显酸性,pH值是开始时大于7逐渐的减小到7然后小于7,故图象与实验操作过程相对应.
B、在一定温度下,向一定量接近饱和的硝酸钾溶液中不断加入硝酸钾晶体,硝酸钾晶体继续溶解至饱和,溶液的溶质质量变大,达饱和后硝酸钾不再溶解,溶液的质量分数不再改变;变化曲线表明,随着硝酸钾晶体的不断加入,溶液的质量分数不断增大,到了一定程度,该溶液的质量分数保持不变,故图象与实验操作过程不相对应.
C、由于锌比铁活泼,与酸反应速度快,图象的斜率锌应比铁大;等质量的铁生成是氢气要比锌生成的氢气多,图象的终点应该比锌高,故图象与实验操作过程不相对应.
D、向HCl和CaCl2的混合溶液中加入Na2CO3溶液时,Na2CO3溶液先与盐酸反应生成氯化钠、水和二氧化碳,开始时不会生成沉淀,盐酸消耗完再与CaCl2反应会生成碳酸钙沉淀,故沉淀的量先是零,在不断上升,最后形成一条水平直线,故图象与实验操作过程对应.
故选:AD.
点评 此题是对物质的变化过程与图象结合题的考查,对反应过程的详细分析并结合图象走势是解题的关键,是一道培养学生分析问题的好题.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 溶液中的溶剂一定是水 | |
| B. | 可燃物燃烧一定同时满足与O2接触,温度达到着火点 | |
| C. | 酸、碱中一定含有氧元素 | |
| D. | 不能使酚酞试液变红的溶液一定是酸溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是美丽的石笋和钟乳石,在其形成过程中发生多个化学反应,其中一个化学反应时:CaCO3+X+H2O=Ca(HCO3)2,则X的化学式为( )
如图是美丽的石笋和钟乳石,在其形成过程中发生多个化学反应,其中一个化学反应时:CaCO3+X+H2O=Ca(HCO3)2,则X的化学式为( )| A. | CH2 | B. | CO2 | C. | C2H2 | D. | CO |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
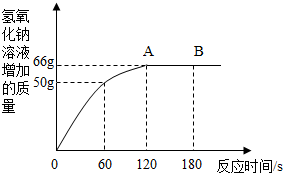 家庭中长期使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,可用酸溶液来清除水垢.小明同学想通过实验测定水垢中碳酸钙的含量,他将过量的稀盐酸加入到200g水垢中(假定水垢中杂质不与酸反应),并将产生的CO2气体全部通入到足量的NaOH溶液中(不考虑盐酸的挥发性),NaOH溶液增加的质量与反应时间的关系如图所示,
家庭中长期使用的热水壶底部有一层水垢,主要成分是碳酸钙和氢氧化镁,可用酸溶液来清除水垢.小明同学想通过实验测定水垢中碳酸钙的含量,他将过量的稀盐酸加入到200g水垢中(假定水垢中杂质不与酸反应),并将产生的CO2气体全部通入到足量的NaOH溶液中(不考虑盐酸的挥发性),NaOH溶液增加的质量与反应时间的关系如图所示,查看答案和解析>>
科目:初中化学 来源: 题型:解答题
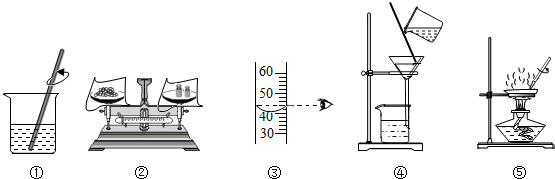
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com