
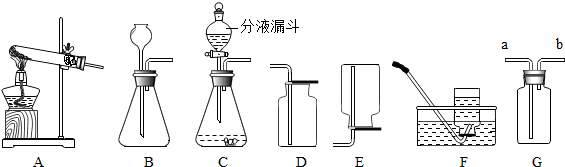
分析 (1)根据装置的选择依据以及特点结合氧气的性质来分析;
(2)根据收集气体的方法以及二氧化碳的性质来分析.
解答 解:(1)用过氧化氢溶液与二氧化锰混合氧气,属于固液常温下制取气体,为了控制反应速率,应选择装置C来制取;氧气的密度比空气大,所以氧气从长管进入,故填:C;a;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(2)因为二氧化碳的密度比空气大,且能溶于水,所以收集二氧化碳一般用向上排空气法,而不用向下排空气法或排水法,故填:二氧化碳的密度比空气大,且能溶于水.
点评 本题考查的是气体的制取与收集的知识,完成此题,可以依据已有的气体制取与收集的知识进行.


科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 结论 | |
| 步骤A | 将加热后的固体放入水中,搅拌、静置. | 底部有大量白色不溶物 | 剩余固体中含有碳酸钙 |
| 步骤B | 取上层清液,滴加无色酚酞试液. | 变 红 | 剩余固体中含有CaO |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 如表是固体A的溶解度.向100g水 中不断加入固体A或改变温度,得到相应的溶液①~⑤.请回答:
如表是固体A的溶解度.向100g水 中不断加入固体A或改变温度,得到相应的溶液①~⑤.请回答:| 温度/℃ | 20 | 30 | 40 | 50 | 60 |
| A溶解度/g | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 |

查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ①②③ | C. | ③④ | D. | ②③ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

 ,写离子符号S2-,该元素的原子核外有3个电子层,它属于非金属元素(填“金属”或“非金属”),在化学反应中易得到(填“得到”或“失去”)电子.
,写离子符号S2-,该元素的原子核外有3个电子层,它属于非金属元素(填“金属”或“非金属”),在化学反应中易得到(填“得到”或“失去”)电子.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①④⑤ | C. | ④①③④ | D. | ②②③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com